为什么你的口罩发美国老有问题?口罩发美国到底该做什么认证?口罩发美国该注意哪些细节?
 2092
2092当地时间4月20日,据美国《洛杉矶时报》报道,近日,比亚迪获得了美国加利福尼亚州近10亿美元的口罩订单。相信这几天应该所有朋友们都被这个新闻刷爆了朋友圈。
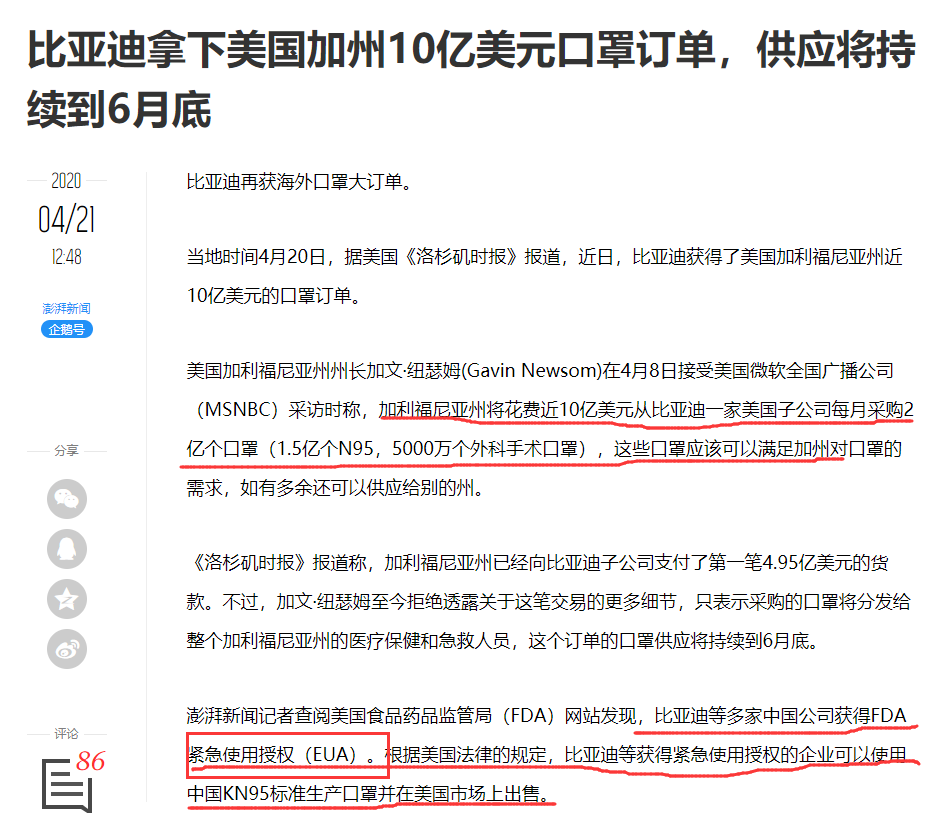
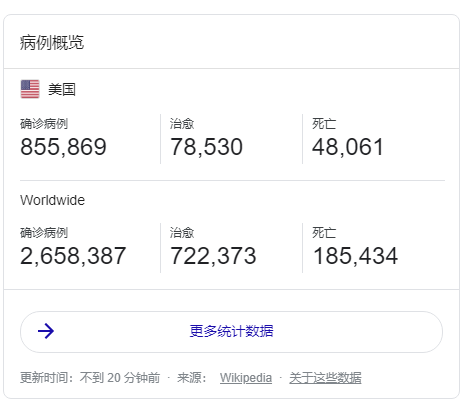
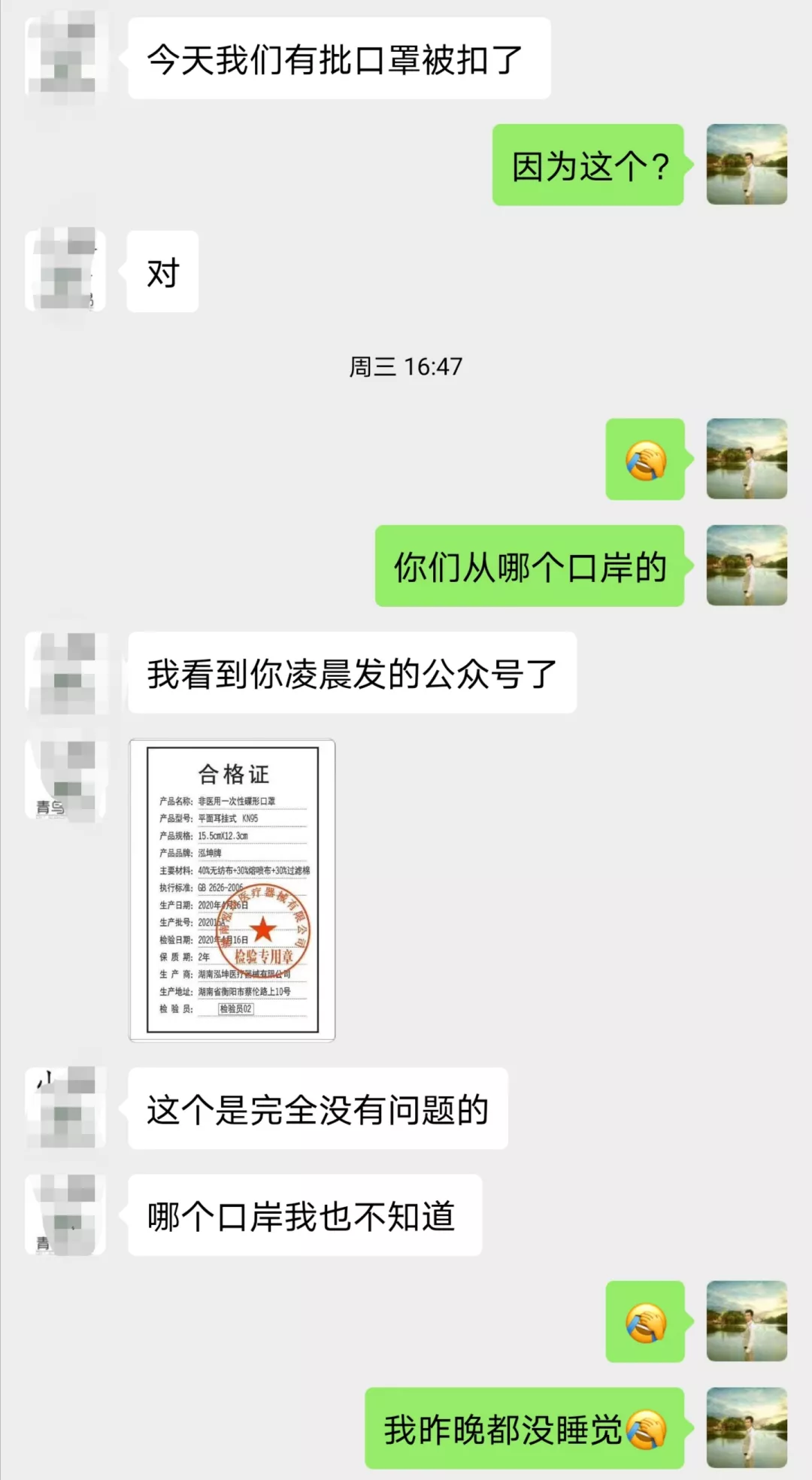
因此,不仅比亚迪得到了美国加州政府的10亿元大订单,其他外贸的朋友应该也接到了不少来自美国的询价,最直接的表现在于,包括小编在内,最近接到的发往美国LAX,JFK,ORD,MIA的询价越来越多,往这个方向的包机现在也越来越多。疫情如此紧急,我们非常希望口罩等防疫物资能够顺利最快能够发往美国。但是,最近令绝大部分货代和外贸的朋友崩溃的事情是,一边是客户着急要口罩,一边是在出口报关环节,口罩等防疫物资频频被查验扣货甚至是退回,每天外贸货代的朋友最揪心的事情就是手上的防疫物资到底能不能顺利发出去。
以发美国为例,小编跟大家解析为什么大家发美国的防疫物资频频出现问题。
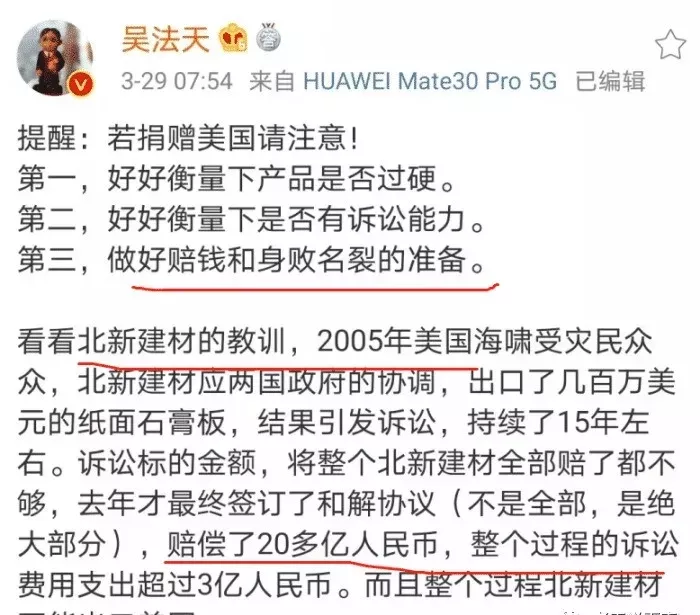
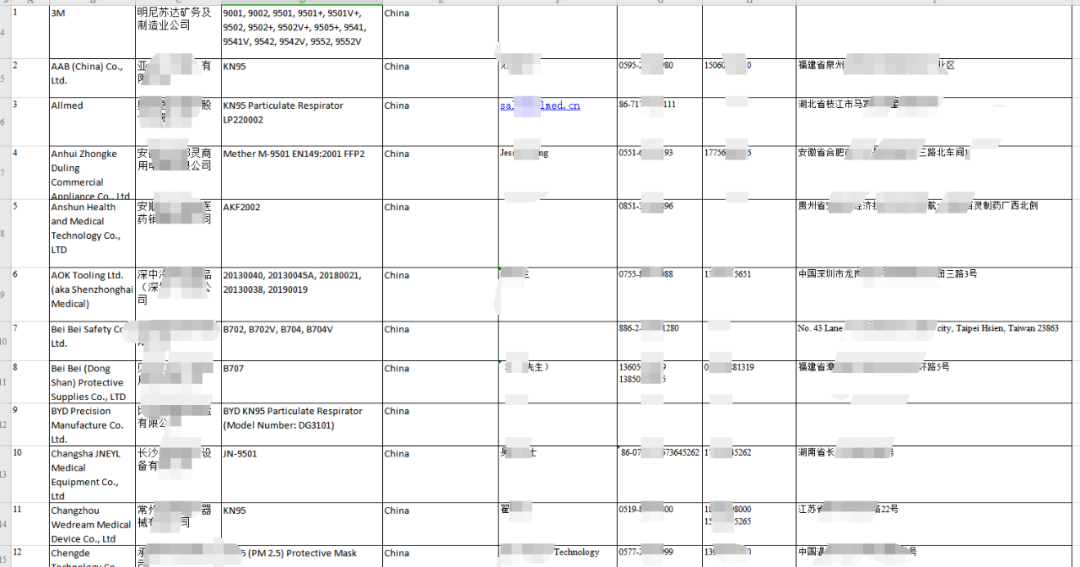
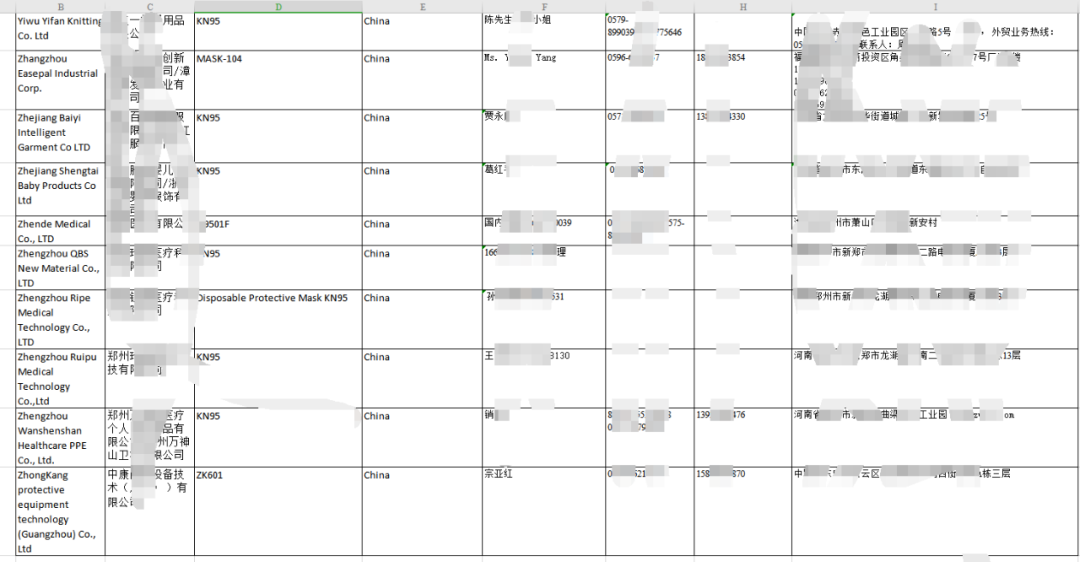
由于医用口罩出口及目的地国家的要求都非常严格,所以医用口罩基本上都是从药监局名单上面的工厂采购的物资,基本上都是资质齐全包装合格的产品,出现问题的概率反而很少,出现问题的重灾区在于非医用物资,因为根据海关相关规定,非医用口罩上面不能出现任何医用的信息,包括但不局限于FDA标识/医用十字标识/中英文医用/medical等信息,中英文医用/medical等信息经过各家货代一再的强调下,现在已经改观了很多,这一块的问题已经基本上慢慢规范,医用十字标识容易被大家遗漏,而FDA标识则成为了问题的重灾区,原因有两个: 工厂不专业,认为有FDA就是好,于是在包装上面已经批量印好FDA标识,导致很难更改。 美国客户自己要求要有FDA(跟海关要求好像有点冲突)。 (三)检测报告。海关只接受国际标准的检测报告,不接受行业标准的,必须要有MA/CNAS等这些组织的LOGO的检测报告才可以,合格的检测报告封面如下: (四)CE标识,CE标识是欧盟要求的,去非欧盟国家包括美国就不要印上这个CE标识了,一旦印上CE标识,海关就需要找到对应的信息来支持这个CE标识对应的是非医用EN149的标准,一旦没有任何信息可以支持,扣货。 那既然我国海关要求非医用口罩不能有FDA标识,而客户又要求有FDA认证,这个不是有冲突吗? 客户其实不是不懂,是因为客户也很明白中国的工厂做NIOSH检测注册的太少,FDA的认证也乱七八糟,但是至少他们能够辨别,有FDA注册号,至少在清关环节,他们不会碰到麻烦,后期进入美国市场销售,也不会担心后期被美国政府开巨额罚款,美国政府擅长“秋后算账”,这个大家应该都有听说。如果资质证书不齐全,连捐赠都会被美国政府起诉,特殊时期,美国政府对口罩物资的销售监管会更加严格,销售没有资质认证的口罩,美国政府可以让你倾家荡产和身败名裂。 看明白了这个点之后,你就应该清楚,中国海关卡得严格,其实也是对大家好,那到底我们的KN95口罩,一次性三层平面口罩,应该怎么样才能符合美国的进口要求,且先看NIOSH和FDA到底是什么样的机构。 (一)NIOSH 如果小编理解的没错的话,也就是一句话:医用口罩做FDA认证,防护口罩做NIOSH检测注册,如果防护口罩没有做NIOSH检测注册,至少要做510K豁免的注册模式,客户要求工厂要有FDA很大程度上就是这个。(据了解NIOSH不接受一次性平面民用口罩的检测注册,所以一次性平面口罩还是按510K豁免的注册模式做FDA注册认证登记) 那如果没有NIOSH检测注册,又没有FDA注册认证怎么办?因疫情影响,现针对中国KN95型口罩的EUA申请,FDA在短期内快速审核口罩资料,并在官网公布获得EUA授权的企业和产品型号,相当于发一个临时简易合格证替代NIOSH认证。



































当地时间4月20日,据美国《洛杉矶时报》报道,近日,比亚迪获得了美国加利福尼亚州近10亿美元的口罩订单。相信这几天应该所有朋友们都被这个新闻刷爆了朋友圈。


因此,不仅比亚迪得到了美国加州政府的10亿元大订单,其他外贸的朋友应该也接到了不少来自美国的询价,最直接的表现在于,包括小编在内,最近接到的发往美国LAX,JFK,ORD,MIA的询价越来越多,往这个方向的包机现在也越来越多。疫情如此紧急,我们非常希望口罩等防疫物资能够顺利最快能够发往美国。但是,最近令绝大部分货代和外贸的朋友崩溃的事情是,一边是客户着急要口罩,一边是在出口报关环节,口罩等防疫物资频频被查验扣货甚至是退回,每天外贸货代的朋友最揪心的事情就是手上的防疫物资到底能不能顺利发出去。
以发美国为例,小编跟大家解析为什么大家发美国的防疫物资频频出现问题。
由于医用口罩出口及目的地国家的要求都非常严格,所以医用口罩基本上都是从药监局名单上面的工厂采购的物资,基本上都是资质齐全包装合格的产品,出现问题的概率反而很少,出现问题的重灾区在于非医用物资,因为根据海关相关规定,非医用口罩上面不能出现任何医用的信息,包括但不局限于FDA标识/医用十字标识/中英文医用/medical等信息,中英文医用/medical等信息经过各家货代一再的强调下,现在已经改观了很多,这一块的问题已经基本上慢慢规范,医用十字标识容易被大家遗漏,而FDA标识则成为了问题的重灾区,原因有两个: 工厂不专业,认为有FDA就是好,于是在包装上面已经批量印好FDA标识,导致很难更改。 美国客户自己要求要有FDA(跟海关要求好像有点冲突)。 (三)检测报告。海关只接受国际标准的检测报告,不接受行业标准的,必须要有MA/CNAS等这些组织的LOGO的检测报告才可以,合格的检测报告封面如下: (四)CE标识,CE标识是欧盟要求的,去非欧盟国家包括美国就不要印上这个CE标识了,一旦印上CE标识,海关就需要找到对应的信息来支持这个CE标识对应的是非医用EN149的标准,一旦没有任何信息可以支持,扣货。 那既然我国海关要求非医用口罩不能有FDA标识,而客户又要求有FDA认证,这个不是有冲突吗? 客户其实不是不懂,是因为客户也很明白中国的工厂做NIOSH检测注册的太少,FDA的认证也乱七八糟,但是至少他们能够辨别,有FDA注册号,至少在清关环节,他们不会碰到麻烦,后期进入美国市场销售,也不会担心后期被美国政府开巨额罚款,美国政府擅长“秋后算账”,这个大家应该都有听说。如果资质证书不齐全,连捐赠都会被美国政府起诉,特殊时期,美国政府对口罩物资的销售监管会更加严格,销售没有资质认证的口罩,美国政府可以让你倾家荡产和身败名裂。 看明白了这个点之后,你就应该清楚,中国海关卡得严格,其实也是对大家好,那到底我们的KN95口罩,一次性三层平面口罩,应该怎么样才能符合美国的进口要求,且先看NIOSH和FDA到底是什么样的机构。 (一)NIOSH 如果小编理解的没错的话,也就是一句话:医用口罩做FDA认证,防护口罩做NIOSH检测注册,如果防护口罩没有做NIOSH检测注册,至少要做510K豁免的注册模式,客户要求工厂要有FDA很大程度上就是这个。(据了解NIOSH不接受一次性平面民用口罩的检测注册,所以一次性平面口罩还是按510K豁免的注册模式做FDA注册认证登记) 那如果没有NIOSH检测注册,又没有FDA注册认证怎么办?因疫情影响,现针对中国KN95型口罩的EUA申请,FDA在短期内快速审核口罩资料,并在官网公布获得EUA授权的企业和产品型号,相当于发一个临时简易合格证替代NIOSH认证。






















 热门活动
热门活动 
 福建
福建 04-23 周四
04-23 周四
 热门报告
热门报告 










