【美国进口清关】FDA 自愿合格进口商计划 VQIP 及常见问题解答
 850
850给你可复用的爆品立项与广告节奏和预算模型
自愿合格进口商计划 VQIP(Voluntary Qualified Importer Program)是 FDA 根据《食品安全现代化法案》FSMA 的要求设立的一项旨在加快人类和动物食品进入美国的审查和通关流程的进口管理计划,旨在对符合高标准供应链安全和合规要求的进口商,申请获准后给予其进口的人用及动物食品在进入美国时的加速审查和通关便利。要参与该计划,进口商必须符合特定资格标准,其中包括其境外供应商须由经 FDA 认可的第三方认证机构 CB(Certification body),依据 FDA 的第三方认证机构认可与认证计划 TPP 进行审计并取得相应的、当前有效的设施认证,以及实施其他措施,以支持 FDA 对其所进口食品安全性和供应链安全性保持高度信心。参与该计划需缴纳年度用户费用(Annual user fee),VQIP 用户费费率标准按 FDA 财政年度计算,并于 8 月份在联邦公报上公布,该费用用于支付 FDA 管理该项目的成本,缴纳费用后所享受的进口快速通关等 VQIP 程序性便利,仅在当个财政年度内有效,即每年 10 月 1 日至次年 9 月 30 日,每年需提交续期申请并续交 VQIP 用户费方可继续参与。自 2018 年初起,符合条件的进口商可通过 FDA 行业系统 FIS(FDA Industry Systems)网站在线提交申请加入 VQIP,进口商在提交 VQIP 申请时,可纳入任意数量的食品,但前提是这些食品来自所申报的境外供应商,且相关生产设施须持有依据 FDA 第三方认证计划(TPP)签发的有效设施认证。
什么是 FDA 自愿合格进口商计划 VQIP
FDA《食品安全现代化法案》FSMA 对《联邦食品、药品和化妆品法案》(FD&C Act)进行了修订,增设了第 806 条(Section 806),即“自愿合格进口商计划”VQIP(Voluntary Qualified Importer Program)(21 U.S.C. 384b)。第 806(a)(1) 条(Section 806(a)(1))要求 FDA 建立以下机制:
(1)一项旨在用于对自愿同意参与 VQIP 的进口商所申报进口的食品实施加快审查与进口放行的计划;以及
(2)一项符合《联邦食品、药品和化妆品法案》第 808 条(Section 808 of the FD&C Act)(21 U.S.C. 384d)规定的程序,用于签发随同参与 VQIP 的进口商所申报进口食品一并使用的设施认证。
根据 FSMA 法案要求设立的 VQIP 是一项自愿参与,需缴纳费用的计划(Voluntary, fee-based program),用于对那些在其供应链食品安全与防护方面已建立并持续保持高度管控水平的进口商所进口的食品,提供加快审查和入境处理。上述管控水平包括但不限于:从已依据 FDA 的“经认可第三方认证计划”(Accredited Third-Party Certification Program)(亦称第三方计划 Third-Party Program 或 TPP)取得认证的设施进口食品〔《联邦食品、药品和化妆品法》(FD&C Act)第 808 条(21 U.S.C. § 384d)〕,并符合《第三方认证机构认可及食品安全审计与认证法规》(即 TPP 法规,见 21 CFR 第 1 篇 M 分篇)的相关要求;同时,还包括其他能够支持 FDA 对其所进口食品安全性与安保性具有高度信心的措施。
VQIP 申请(VQIP application)可涵盖任何受 FDA 监管(FDA-regulated)的人类和/或动物食品,包括但不限于海产品(Seafood)、加工食品(Processed foods)、农产品(Produce)、膳食补充剂(Dietary supplements)和宠物食品(Pet food)。纳入 VQIP 申请范围的食品,必须由经 FDA 认可的第三方认证计划(FDA’s Accredited Third-Party Certification Program)下获得资质的审计机构认证的外国设施(Foreign facility)或农场(Farm)生产。该认证计划同样由《食品安全现代化法案》FSMA 强制要求,旨在为第三方审计机构(Third-party auditors)提供认证途径,使其能够对外国实体及其生产的人类和动物食品进行食品安全审核并颁发认证。这些审核(Audits)证明该设施或农场已满足适用的食品安全要求。
VQIP 申请被获准之后,FDA 通过其在 PREDICT 系统中预设的规则,能够自动识别 VQIP 申请中涵盖的食品批次,美国海关的 ACE/DIS/ITACS 系统在大多数情况下会给予立即放行。美国政府使用自动化商业环境 ACE 系统来处理进出口业务,ACE 允许企业以电子方式提交所需数据,从而简化进出口流程。
FDA 通常仅在存在合理依据(For cause)的情况下,对经批准的 VQIP 食品进行检查和抽样,例如当 FDA 怀疑存在可能危害公共健康的风险时,如潜在污染或标签不实(Misbranding)。但如果 FDA 确实需对 VQIP 食品进行检查或抽样,检查或检验地点将在可行范围内安排在 VQIP 食品的目的地或进口商指定的其他地点。如果 FDA 对 VQIP 食品进行抽样,相关样本的实验室检测将予以优先处理。通过对符合条件的进口食品实施加快放行,该机制旨在激励进口商建立健全的供应链管理体系,在提升进口食品安全水平的同时,由于 VQIP 食品具有既定的安全标准,使得 FDA 能够将有限的监管资源集中于对公共健康构成更高潜在风险的食品进口上。
要申请参与 VQIP 计划,进口商应至少具有 3 年向美国进口食品的历史,并在适用情况下,遵守《外国供应商验证计划》FSVP(Foreign Supplier Verification Program)、果汁 HACCP 和/或海产品 HACCP 法规项下的供应商验证及其他责任。参与 VQIP 的关键在于制定并实施一套质量保证计划 QAP(Quality Assurance Program),其中应包括与食品安全和食品防护相关的书面政策和程序(Written policies and procedures)。
有意申请的进口商可通过 FDA 行业系统 FIS(FDA Industry Systems)网站:https://www.access.fda.gov/ 创建账户,在 FSMA 计划选项下选择 VQIP 提交申请。
登录 FIS 系统后,从 FSMA Programs 的可用系统列表中选择“Voluntary Qualified Importer Program”,
系统将引导你进入 VQIP 页面,选择屏幕左侧的“参与意向通知”(Notice of Intent to Participate)选项,以告知 FDA 你有意参与该计划。必须“参与意向通知”才能申请新财政年度的 VQIP 程序性便利(Benefits)且该意向通知需每年重新提交,
你的公司名称(Firm name)和该机构(Agency)当前接受 VQIP 申请的财政年度将显示在主屏幕上。选择“提交参与意向通知”将你的通知发送给 FDA,
提交意向通知后,系统将返回 VQIP 主页并将显示“创建申请”(Create Application)菜单选项,选择“创建申请”以开始申请流程。
FDA 将审核进口商提交的 VQIP 申请及所有相关文件,以确定其是否符合 VQIP 资格标准。FSMA 法案第 806(d) 条(Section 806(d))规定,在审查并对 VQIP 申请作出决定时,FDA 必须基于包括外国供应商的合规历史记录以及进口商的食品安全实践在内的因素,评估拟进口食品的风险水平。若进口商被获准加入该计划,FDA 将进行检查(Inspection),以核实其是否符合资格标准,并已全面落实 QAP 中规定的食品安全和食品防护条款(Provisions)(需要注意的是,食品防护条款不适用于动物食品(Animal food))。检查(Inspection)将包括审查书面程序及记录,以验证是否符合 VQIP 规定(VQIP directives)。
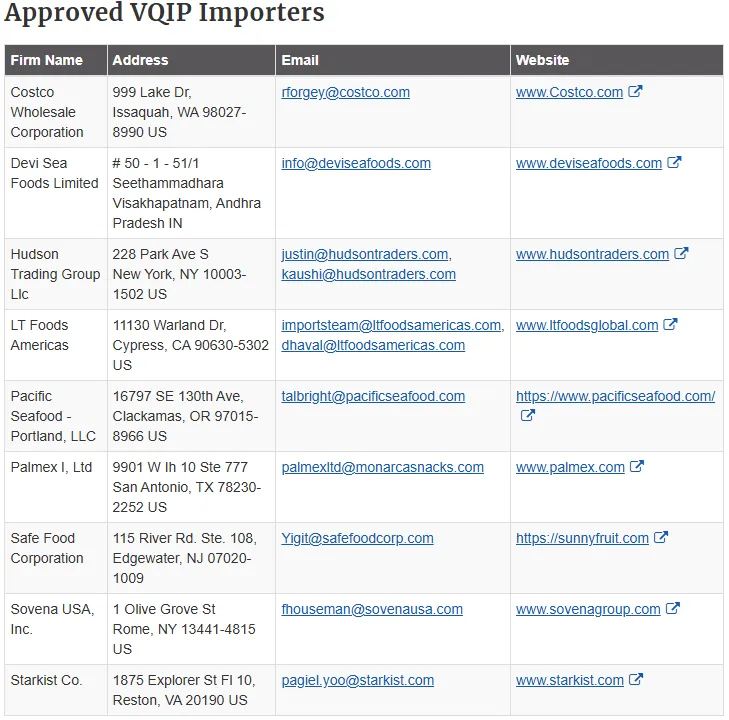
FDA 财年经批准的 VQIP 进口商会发布在 FDA 官网的 VQIP 进口商公开列表中,VQIP 进口商可以选择不列入 VQIP 进口商名单。VQIP 进口商选择不列入公开发布的获准 VQIP 进口商名单,不会对其 VQIP 计划参与资格产生任何影响。
FDA 自愿合格进口商计划 VQIP 常见问题解答
进口商是否只需提交一份申请即可涵盖其进口的不同食品?
是的。进口商只需提交一份申请,即可涵盖其希望根据 VQIP 计划进口的所有不同食品。该申请可涵盖多个外国供应商设施或农场,以及相应食品。与这些食品相关的整个供应链信息(包括外国供应商、FSVP 或 HACCP 进口商以及申报人/报关行)均包含在这一份申请中。
如果进口商已满足 FSMA 强制规定的 FSVP 规则的要求,是否就基本满足 VQIP 要求?
进口商必须遵守 FSVP 的要求,确保所进口食品的生产方式符合美国相关安全标准。但这并不等同于满足全部要求。VQIP 作为一项自愿性项目,认可的是那些在 FSVP 或 HACCP 强制要求之上,进一步对其供应链建立额外控制措施的进口商。例如,VQIP 进口商必须取得其供应商的设施认证,该认证须由经 FDA 认可的第三方审计机构签发。此外,其 QAP 还应体现其在运输安全和食品防护方面符合其他相关标准。
参与 VQIP 的进口商能够获得哪些便利(Benefits)?
(1)更便捷,更简便的报关入境
FDA 将对经批准的 VQIP 申请中所涵盖的全部食品给予加快进入美国的进口审查与放行处理。
美国食品药品监督管理局 FDA 将通过其基于风险预测的动态进口合规性目标评估 PREDICT(Predictive Risk-based Evaluation for Dynamic Import Compliance Targeting)进口筛查工具(Import screening tool),识别已获批准的 VQIP 申请范围内的食品货物批次(Shipments)。该筛查系统将被设置为在识别相关货运后,在大多数情况下立即予以放行(Immediately release)无需进一步接受检查和/或抽样(Examination and/or sampling);但如基于下文所列的公共健康原因有必要进行检查或抽样的,FDA 仍可对货物实施相应的检查与取样(Examination and sampling)。
(2)有限度的检查和抽样
FDA 将仅在以下情形下,对纳入 VQIP 的食品进口申报实施检查和/或抽样(Examination and/or sampling):
存在明确原因的情形(例如,对食源性疾病暴发或患病事件的调查); 为获取在统计学上必要的、基于风险评估的微生物样本,以通过非偏向性的监测抽样建立或完善产品风险特征;以及 对极小比例的 VQIP 涵盖的进口货物批次进行合规审计,以核实在 VQIP 入境申报(VQIP entry)中声明的产品与 VQIP 申请所涵盖的产品是否一致。
(3)FDA 在优先选择地点(Preferred location)进行检查与取样
当 FDA 需要对纳入 VQIP 的进口申报(Entry)实施检查(Examine)时,FDA 将在可行范围内,尽量在 VQIP 食品的最终目的地或 VQIP 进口商偏好的其他地点进行检查并采集样品。如相关进口申报(Import entry)被拒绝进入美国,FDA 将协助进口商向美国海关和边境保护局 CBP 提出申请,以便从进口商所偏好的港口将被拒绝的产品予以出口。
(4)更快的实验室检测结果
若美国食品药品监督管理局 FDA 对 VQIP 食品进口批次(VQIP food import entry)进行抽样检测,FDA 实验室将优先处理 VQIP 样品。
总的来说,FDA 对已获准加入 VQIP 计划给予的 VQIP 程序性便利(VQIP benefits)指的是 FDA 基于风险评估,对符合 VQIP 要求的进口食品在“进口审查和执法资源分配上给予优先与简化”的制度性待遇,于 VQIP 申请获准后的 10 月 1 日生效,并持续至次年 9月 30 日结束(VQIP 年度)。
参与 VQIP 的资格标准是什么?
进口商(Importers)(指将食品从外国引入美国,或促使食品从外国被引入美国的个人或企业)需满足 FDA 规定的特定资格标准才能申请参与 VQIP,包括:
(1)申请人须具有至少 3 年向美国进口食品的历史记录。该进口历史基于申请人进口的全部食品,包括拟不纳入 VQIP 申请范围的食品。如果申请人进口食品历史超过 3 年,美国食品药品监督管理局 FDA 可能会根据需要审查额外的年份,以充分评估其合规历史记录。
(2)申请人须拥有邓白氏 D&B(Dun & Bradstreet)数据通用编号系统 DUNS(Data Universal Numbering System)编号。
(3)申请人应使用无纸化报关申报人/报关行(Paperless filers/brokers),且该申报人/报关行在其最近一次 FDA 申报人评估(FDA Filer Evaluation)中获得可接受的评级。申报人/报关行(Filer/broker)负责将进口食品报关单(Import entry)和报关汇总表(Entry summary)数据提交至自动化商业环境 ACE(Automated Commercial Environment),并根据需要将进口文件(Import documents)提交至国际贸易辅助通讯系统 ITACS(International Trade Auxiliary Communication System)或通过美国海关 CBP 的文件图像系统 DIS(Document Imaging System)进行提交。
(4)在提交 VQIP 申请时,申请人所进口的任何食品(包括不拟纳入 VQIP 的食品)均不得处于进口预警(Import alert)或 I 类召回(Class I Recall)状态。
(5)申请人及与 VQIP 食品相关的非申请实体,均不得处于正在进行的 FDA 行政或司法行动之中(例如,进口预警、禁令、进口资格取消),亦不得存在未完成适当纠正措施的重大食品安全不合规记录(例如,FDA 检查分类为“需采取官方行动”OAI(Official Action Indicated);一项或多项与食品安全相关的自愿 I 类召回)。注:“非申请实体”(Non-applicant entities)是指与 VQIP 食品相关的、在整个供应链中开展必要活动以确保满足 VQIP 资格要求的实体。与 VQIP 食品相关的非申请实体包括但不限于:该食品的 FSVP 或 HACCP 进口商(若非你本人)、该食品的外国供应商,以及进口申报人/报关行(Import entry filer/broker)。
(6)如申请人为 VQIP 食品的 FSVP 或 HACCP 进口商(即食品进入美国时作为美国所有者或收货人(Owner or consignee),或作为外国所有者/收货人的美国代理/代表),应符合适用的 FSVP、果汁 HACCP(Juice HACCP)或水产品 HACCP(Seafood HACCP)法规规定的供应商验证及其他进口商责任要求。
如申请人并非 VQIP 食品的 FSVP 或 HACCP 进口商,则必须确定该食品的 FSVP 或 HACCP 进口商,并确保其符合适用的 FSVP 或 HACCP 法规要求。
(7)对于拟在 VQIP 计划下进口的食品,其每个外国供应商均须具备当前有效的设施认证(Facility certification)。根据美国食品药品监督管理局 FDA 的经认可的第三方认证(Accredited Third-Party Certification)TPP 法规要求,所有拟根据 VQIP 计划进口的外国食品供应商均需提供有效的设施认证。对于生鲜农产品(Raw produce),则必须提供农场认证(Certification for the farm)。
(8)申请人须制定并实施 VQIP 质量保证计划 QAP(Quality Assurance Program),且该计划的相关文件应随 VQIP 申请(VQIP application)一并提交。
(9)在过去 3 年内,申请人未曾因其进口或拟进口的 FDA 监管产品,在食品安全或供应链安全方面受到美国海关和边境保护局 CBP 的处罚(Penalties)、没收(Forfeitures)或制裁(Sanctions)。
(10)在每个获准参与 VQIP 的财年,申请人须在 VQIP 财政年度开始前的 10 月 1 日之前缴纳相应的用户费用(User fee)。
参与 VQIP 是否需要缴纳用户费用(User fee)?
需要。《联邦食品、药品和化妆品法案》第 743 条(21 U.S.C. 379j-31)规定,所有参与 VQIP 计划的进口商均需缴纳用户费(User fee),以支付 FDA 管理该项目的成本。FDA 将按年度向你收取 VQIP 用户费,费用适用于你获准参与的每个 VQIP 财政年度(Fiscal year)。在 FDA 批准你的申请后,你必须在 10 月 1 日(VQIP 财政年度开始前)之前缴纳用户费,方可享受该财政年度的 VQIP 程序性便利。
为什么参与 VQIP 需缴纳用户费用(User fee)?
参与 VQIP 的年度用户费(Annual user fees)用于支付 FDA 管理该计划的成本。这些成本包括:申请审核费用;对已获准加入该计划的进口商(包括外国和美国国内进口商)进行检查的费用;以及年度信息技术 IT(Information Technology)维护费用。用户费费率将在每个财政年度进行核算,并将于每年 8 月 1 日或之前在《联邦公报》公告中发布。
如果我未在 10 月 1 日前缴纳 VQIP 用户费用(User fee),会怎样?
如果你未在 10 月 1 日前缴纳用户费,则不具备参与 VQIP 的资格。在你的 VQIP 申请获得批准的第一年,如果你未在 10 月 1 日前缴纳用户费用,则你的 VQIP 程序性便利(VQIP benefits)不会在 10 月 1 日生效;若之后补缴,FDA 将在收到全额付款后启动你的权益。在后续年度,如果你未在 10 月 1 日前缴纳用户费用,FDA 将向你发出《拟撤销参与资格通知》(Notice of Intent to Revoke)。若你在通知发出之日起 30 日内仍未缴费,FDA 将正式撤销你参与 VQIP 的资格。
如果 FDA 发现可能影响我参与 VQIP 资格的偏差(Deviations),是否会退还用户费用(User fee)?
否。如果 FDA 发现可能影响你参与 VQIP 资格的偏差,将向你发出《拟撤销参与资格通知》(Notice of Intent to Revoke),并给予你 30 天的整改期限。
如果我退出 VQIP 计划,或 FDA 撤销我参与 VQIP 的资格,是否会退还用户费用?
否。无论出于何种原因,FDA 均不会退还 VQIP 用户费用。
在哪里可以查询当前及往年 VQIP 用户费用(User fee)标准?
FDA 将在每年 8 月 1 日或之前通过《联邦公报》(Federal Register)发布下一 VQIP 财政年度的用户费用标准公告。
当前及历年 VQIP 财政年度的用户费用标准(User fee rates),也可在 FDA 官网 VQIP 用户费用页面查询。
如何申请加入 VQIP 计划?
在 FDA 行业系统 FIS 网站上创建账户。 在美国东部时间 1 月 1 日至 9 月 1 日晚上 11:59 之间提交 VQIP 参与意向通知(Notice of Intent to Participate)。 支付用户费用(User fee)后在 FIS 系统开始 VQIP 申请流程。
我需要提供哪些信息才能完成 VQIP 申请?
VQIP 进口公司(VQIP Importing Firm)识别信息 外国供应商验证计划 FSVP(Foreign Supplier Verification Program)联系信息 VQIP 质量保证计划 QAP(Quality Assurance Program)文件(需符合 FDA《自愿合格进口商行业指南》规定的要求) 申报人/报关行联系信息 外国供应商联系信息及食品清单
VQIP 计划下允许哪些类型的食品?
食品必须来自经 FDA 认可的第三方认证机构认证,符合相关食品安全规范的工厂(或农场); 申请人进口的任何食品,包括不属于 VQIP 计划范围的食品,均不得处于进口预警(Import alert)或 I 类召回状态(Class 1 recall)。
美国食品药品监督管理局 FDA 是否会加快对混合报关(Mixed entry)中包含的 VQIP 食品的报关处理(即报关 Entry 中包含 VQIP 食品和我的 VQIP 未涵盖食品)?
对于包含 VQIP 食品与未参与 VQIP 计划的食品的混合进口申报(即同一进口申报中同时包含 VQIP 食品和不在 VQIP 计划涵盖范围内的食品),FDA 仅会对其中的 VQIP 食品予以加快审查与放行。未参与 VQIP 计划的食品仍将按 FDA 的常规进口审核程序进行处理,包括在适用情况下接受例行检查与抽样(Routine examination and sampling)。因此,将 VQIP 食品与非 VQIP 食品合并在同一进口申报中,可能会延缓 VQIP 食品的报关放行。
入境申报时应提交哪些信息以识别 VQIP 食品?
除了进口过程中通常需要提交的申报数据要素外,你还应提供 VQIP 合规性声明 AofC 代码(Affirmation of Compliance)和你的 VQIP 申请编号(VQIP application number),以标识该报关 Entry 进口商品为 VQIP 食品。对于每一票 VQIP 食品报关(VQIP food entry),申报人应确保进口申报信息(Import entry information)与 VQIP 申请中所列食品信息一致,包括 FDA 产品代码。FDA 产品代码(FDA product code)用于描述特定产品,由 5 至 7 位数字与字母组合构成。FDA 产品代码应与产品名称和/或商业发票描述一致,并应与依据第三方认证计划 TPP 向外国供应商签发的设施认证中所列该产品的产品代码一致。
在什么情况下 FDA 会对 VQIP 食品进行检查或抽样(Examine or sample)?
当 FDA 判断某种 VQIP 食品存在或可能存在公共健康风险时,则该食品可能会被进行“有因”(For cause)检查(Examination)。例如,在对某一类食品或某一外国供应商(其产品涵盖于已获批准的 VQIP 申请中)相关的疫情或疾病进行调查期间,即使没有具体信息表明某一票 VQIP 食品涉及该疫情或疾病,FDA 仍可能对该 VQIP 食品进行检查和取样。在某些情况下,VQIP 食品也可能因特定的、基于风险的监测任务而接受微生物抽样(Microbiological sampling)。然而,对 VQIP 食品的监测性抽样(Surveillance sampling)将被列为低优先级(Low priority);如果 FDA 能够从非 VQIP 食品中获得具有充分统计学意义、无偏的样本,则可能完全不对 VQIP 食品进行此类抽样。如确需对 VQIP 食品进行监测性抽样,FDA 将在该食品完成进口放行并进入美国国内流通后采集样本(即作为美国国内进口样本采集)。FDA 亦可能定期开展合规审计检查(Audit examinations),以核实进口商对 VQIP 要求的遵守情况,该类检查可能包括取样及与食品风险相关的标签审核。此类审计检查所采集的样本同样将作为美国国内进口样本采集。因此,监测性抽样(Surveillance sample collection)的实施不会延误 VQIP 食品的进口放行。在可行范围内,并依据公共健康优先事项(Public health priorities),FDA 实验室将对在调查过程中采集的 VQIP 食品样本安排优先检测。FDA VQIP 进口商帮助台(FDA VQIP Importers Help Desk)亦将提供支持,协助了解正在接受审查或检测的 VQIP 食品状态,以尽量减少延误。
谁可以参加 VQIP 计划?
参与 VQIP 的主体必须是食品进口商(Food importer)。就 VQIP 而言,进口商是指将食品从外国引入美国关境(Customs territory),或促使食品被引入美国关境的个人或实体(《联邦食品、药品和化妆品法案》第 806(g) 条)(Section 806(g) of the FD&C Act)。VQIP 进口商可以位于美国境外。可能作为 VQIP 进口商的主体包括食品的制造商(Manufacturer)、所有者(Owner)、收货人(Consignee)以及备案进口商(Importer of record),前提是该进口商能够满足 FDA 所要求的全部 VQIP 参与标准。
我是否必须是海关备案进口商(Importer of Record)才能作为 VQIP 进口商?
作为 VQIP 进口商,你可以同时也是 CBP 的备案进口商,但并非必须。CBP 对食品的备案进口商的定义是:负责为该食品办理进口申报(Making entry)并缴纳进口关税、费用和税款的个人或公司。根据《美国法典》第 19 编第 1484(a)(2)(B) 条(19 U.S.C. 1484(a)(2)(B)),备案进口商可以是食品的所有者或购买方,或者在所有者、购买方或收货人指定的情况下,也可以是经 CBP 许可的报关行(Broker)。
VQIP 进口商是否与其他适用于食品进口商的 FDA 法规项下的进口商相同?
VQIP 进口商可以与“外国供应商验证计划”FSVP(Foreign Supplier Verification Program)法规或果汁和水产品“危害分析与关键控制点” HACCP(Hazard analysis and critical control point)法规中定义的进口商为同一主体,但并非必然相同。FSVP 或 HACCP 进口商是指就某一特定食品而言,适用 FDA 的 FSVP 法规(21 CFR part 1, subpart L)或果汁/水产品 HACCP 法规中关于进口商要求的进口商(分别见 21 CFR 120.14 和 123.12)。根据 FSVP 和 HACCP 进口商法规(Importer regulations),进口商是指在食品进入美国时的美国所有者或收货人,或在进口时作为外国所有者或收货人的美国代理或代表(见 21 CFR 1.500(FSVP);21 CFR 120.3(h)(果汁 HACCP);和 21 CFR 123.3(g)(水产品 HACCP))。FSVP 或 HACCP 进口商必须位于美国境内。当某一食品的 FSVP 或 HACCP 进口商为外国所有者或收货人的美国代理或代表时,该美国代理或代表应负责履行与该食品相关的 FSVP 或 HACCP 要求。
然而,VQIP 进口商不要求位于美国境内。如果位于美国的 VQIP 进口商同时也是该食品的 FSVP 或 HACCP 进口商,则其应当遵守适用的 FSVP 或 HACCP 法规要求。否则,VQIP 进口商应当确保由相应的 FSVP 或 HACCP 进口商履行适用的法规要求。
我是否可以从任何外国供应商采购通过 VQIP 进口的食品?
可以。申请人可以从任何外国供应商采购其在 VQIP 计划下进口的食品,前提是该外国供应商未因进口预警(Import Alert)而被实施无需实物查验的扣留 DWPE(Detention without physical examination),并且持有依据 FDA 第三方认证计划 TPP 法规,由经 TPP 认可的认证机构(亦称审计机构)签发的、当前有效的食品设施认证。
就 VQIP 而言,“外国供应商”(Foreign supplier)的含义与《外国供应商验证计划》FSVP 法规中的定义一致,即:对于某一食品,是指制造或加工该食品、饲养该食品所来源动物,或种植该食品,并将其出口至美国,且在出口前未再由其他设施进行进一步制造或加工的机构(Establishment);但仅限于加贴标签或其他类似的、影响极小(De minimis)的进一步加工活动除外(参见 21 CFR 1.500 中“Foreign supplier”的定义)。
为什么我需要至少 3 年向美国进口食品的经验才能参与 VQIP?
FDA 认为,至少 3 年的食品进口历史是对 VQIP 申请进行充分评估所需的最低期限。FDA 将审查你在过去 3 年内进口至美国的所有食品的进口记录,而不仅限于你计划在 VQIP 项下进口的食品。如果你从事食品进口超过 3 年,FDA 可能会根据需要将审查范围延伸至更早的年份,以便充分评估你的合规历史。例如,如果你在过去 5 年内仅偶尔进口食品,FDA 可能会审查你完整的 5 年全部进口记录。又如,若 FDA 在过去 3 年内发现与食品、外国供应商或进口商相关的违规情况,FDA 可能会审查超过 3 年的进口历史,以评估你在实现合规方面所采取的后续纠正措施情况。
我是否需要参与美国海关和边境保护局 CBP 的“海关-贸易反恐伙伴计划”C-TPAT(Customs-Trade Partnership Against Terrorism)才能符合参与 VQIP 的资格?
参加 C-TPAT 并非参与 VQIP 的直接或必要条件。然而,FDA 鼓励申请人参与 C-TPAT,以确保其在 VQIP 计划下进口的食品同时能够享受 CBP 在 C-TPAT 计划下提供的通关放行便利(Entry benefits)。
我需要为外国供应商取得什么样的认证(Certification)?
根据《联邦食品、药品和化妆品法案》第 806(d) 条(Section 806(d) of the FD&C Act)的规定,凡是拟在 VQIP 计划下进口食品的,每一家外国供应商的设施(Facility)均必须取得符合该法案第 808 条(Section 808 of the FD&C Act)要求的设施认证。符合 FD&C Act 法案第 808 条要求的认证,是指依据 FDA 的第三方认证计划 TPP 法规,由经 TPP 认可的认证机构 CB 签发的认证。就 TPP 而言,“设施”并不限于 FD&C Act 法案第 415 条(Section 415 of the FD&C Act)项下需要注册的设施。外国供应商的设施必须通过经 TPP 认可的认证机构实施的监管审计(Regulatory audit),并据此获得设施认证(见 21 CFR 1.651 和 1.653)。该监管审计可由进口商或外国供应商提出申请。
FDA 对外国供应商实施的检查(Inspection)并不符合 FD&C Act 法案第 806(d) 条所规定的认证要求,因为 FDA 检查并不会产生符合第 808 条(Section 808)要求的设施认证(Facility certification)。
什么是设施认证(Facility certification)?
设施认证是指经 FDA 第三方认证计划 TPP 认可的认证机构 CB,在完成监管审计及其他必要活动后,为确认某一设施符合 FD&C Act 法案及 FDA 相关食品安全法规要求而出具的合规证明(Attestation)。
进口商希望纳入 VQIP 计划的任何食品,均应在该设施认证所涵盖的产品范围内。经 TPP 认可的认证机构在向 FDA 提交认证信息(Certification information)时,会同时提交用于描述设施认证所涵盖产品的 FDA 产品代码。经 TPP 认可的认证机构签发的设施认证中所列的 FDA 产品代码应与 VQIP 申请中拟纳入的产品的产品代码相符,以确保相关产品能够适用 VQIP 的程序性便利(VQIP benefits)。
什么是监管审计(Regulatory audit)?
就 VQIP 和 TPP 而言,监管审计是指对符合条件的实体进行的审计(Audit),用于评估该实体是否符合 FD&C Act 法案及 FDA 食品安全法规的相关要求。监管审计的结果将用于判断该设施是否符合获得 FD&C Act 法案第 806 条(Section 806 of the FD&C Act)项下设施认证的资格。
我是否可以根据 VQIP 计划进口初级农产品(Raw agricultural commodity)?
可以。你可以根据 VQIP 计划进口初级农产品,但前提是该农产品所来源的农场(Farm)必须取得由经 TPP 认可的认证机构依据 FDA 第三方认证计划法规签发的、有效的设施认证(Facility certification)。
我是否需要在 VQIP 申请中附上外国供应商设施认证的副本?
不需要。但你必须提供由经 TPP 认可的认证机构为该设施认证分配的认证编号(Certification number)。FDA 将通过该认证编号核实该外国供应商是否持有有效的设施认证。
根据 VQIP 计划进口食品的外国供应商设施,需要多久重新认证一次?
根据《联邦食品、药品和化妆品法案》第 808(d)(1) 条(Section 808(d)(1) of the FD&C Act)的规定,为维持 VQIP 计划下的进口资格,VQIP 食品的外国供应商必须每年重新获得设施认证。根据 FDA 的 TPP 法规,经认可的认证机构可签发有效期最长不超过 12 个月的认证(21 CFR 1.653(b)(1))。在某些情况下(例如季节性生产),根据 TPP 获得认可的认证机构可能签发更短期限的认证,从而需要更频繁地进行审计和重新认证。
如果外国供应商的设施认证在 VQIP 财政年度内到期,我该怎么办?
你有责任确保 VQIP 申请中所依据的所有外国供应商设施认证均处于有效状态。因此,你的外国供应商应妥善管理其设施认证,以确保认证持续有效。你应与你的外国供应商协调,确保在现有认证到期前完成监管审计并取得新的设施认证。若因特殊情况导致外国供应商无法在现有认证到期前取得新的认证,你应及时通知 FDA 其正在办理新的设施认证,并在获得新认证编号后通过修订程序(Amendment process)更新你的 VQIP 申请。如果你在设施认证失效的情况下仍在 VQIP 项下进口食品,FDA 将启动撤销你 VQIP 资格的程序。若你确定在食品生产设施的认证到期后不再计划将相关食品纳入 VQIP,应在认证到期时将该食品从 VQIP 申请中移除。
如何提交申请参与 VQIP?
要提交申请参与 VQIP,你需要:
1,在 FDA 行业系统网站 FIS(FDA Industry Systems):https://www.access.fda.gov/ 创建一个在线账户。你在线账户中的信息将自动填充到你的 VQIP 申请中。
2,美东标准时间 EST(Eastern Standard Time)每年的 1 月 1 日 12:00 a.m. 至 9 月 1 日 11:59 p.m. 期间,须在线提交 VQIP 的参与意向通知(Notice of Intent to Participate)以及下一财政年度(Fiscal year)(自 10 月 1 日起)参与该计划的申请(Section 806(c) of the FD&C Act)。
我需要提供哪些信息才能完成 VQIP 申请?
VQIP 申请分为 A 至 G 部分,具体如下:
A 部分(Section A):申请人及公司信息 B 部分(Section B):外国供应商验证计划 FSVP 与危害分析及关键控制点 HACCP 进口商信息 C 部分(Section C):质量保证计划 D 部分(Section D):申报人/报关行信息 E 部分(Section E):外国供应商设施及食品 F 部分(Section F):备注 G 部分(Section G):摘要 H 部分(Section H):电子签名
要完成申请,你需要提供相关信息,以便准确填写在线 VQIP 申请中各部分的字段。你还需要附上你的 QAP(质量保证计划)。
什么是 DUNS 编号?
DUNS 编号是由 D&B 邓白氏公司提供的、用于识别企业的唯一九位数字编号。经申请,D&B 可为一家企业的每一个实际经营地点(Physical location of a business)分别分配一个 DUNS 编号。
DUNS 编号在 VQIP 申请中如何使用?
在 VQIP 计划中,FDA 将 DUNS 编号作为用于识别你具体经营地点以及你在 VQIP 申请中所列明的每一家非申请实体(例如外国供应商、申报人/报关行以及 FSVP 或 HACCP 进口商)的唯一识别码(Unique identifier)。你需在申请中提供你你自身的 DUNS 编号。此外,你还需为每一家列明的非申请实体提供其地址或 DUNS 编号。如果输入地址,系统将在可用的情况下自动填充相应的 DUNS 编号;如果输入 DUNS 编号,系统将自动填充地址信息。
我的 VQIP 草稿申请在系统中会保存多久?
FDA 会将你的申请草稿(Draft application)在 VQIP 在线申请系统中保留两年,自你上次保存草稿之日起算,直至你完成并提交申请。一旦你完成并提交申请,草稿版本将不再保留。
我是否需要在每个 VQIP 年度重新提交 QAP?
如果你提交 VQIP 申请时,你此前向 FDA 提交的 VQIP 质量保证计划 QAP 未发生任何变化,则无需在每个年度重新提交该 QAP。但你应确保你的 QAP 始终保持最新状态,并在 VQIP 财政年度内如对食品安全或食品防护政策和程序作出任何变更,应及时向 FDA 提交更新。作为申请流程的一部分,你需确认你当前的 QAP 是最新的。
我如何获取用于判断报关行/申报人是否符合 FDA 要求的信息?
FDA 的申报人评估计划(Filer Evaluation Program)用于监测报关行/申报人向 FDA 电子传输的申报数据(Entry data)的准确性。了解其合规状态的最佳方式是与该报关行/申报人建立沟通关系,由其向你提供最近一次 FDA 评估结果。你也可以通过 FDA 公布的申报人评估结果页面查询报关行/申报人合规状态的相关信息。
我能使用不在 FDA 申报人评估结果名单上的报关行/申报人吗?
未列入 FDA 申报人评估结果名单的报关行/申报人,意味着其尚未接受 FDA 的评估。如果在你提交 VQIP 申请时,你的报关行尚未接受 FDA 评估,你或该报关行可向 FDA 申请进行申报人评估(Filer evaluation)。FDA 完成评估后,其结果将被列入 FDA 申报人评估结果名单。若该报关行在 FDA 申报人评估中获得“可接受”(Acceptable)的结果,则你可以在 VQIP 计划下使用该报关行进行申报。
什么是 VQIP 质量保证计划(QAP)?
你的 VQIP 质量保证计划 QAP(Quality Assurance Program)是由一整套书面政策和程序(Written policies and procedures)构成的文件汇编,用于说明你将如何确保对所进口食品的安全性和安全防护具有充分的控制。你可以采用任何形式来组织你的 QAP,只要其能够涵盖你在 VQIP 计划下进口的所有食品,以及与这些食品相关的全部书面政策和程序。
我是否可以使用现有质量保证计划中已成文、且同样适用于 VQIP 的政策和程序?
可以。你可以提交现有的书面政策和程序(Written policies and procedures),只要其符合 VQIP 质量保证计划 QAP 的相关要求。若你提交的 QAP 文件中不仅包含适用于 VQIP 的政策和程序,还包含其他不属于 VQIP 范围的内容,则你应明确标识哪些具体政策和程序是作为 VQIP QAP 提交的。例如,你可以在每一个 QAP 章节下,提供一份对应的文件清单,列明适用文件的名称及其所在页码。你的 QAP 应涵盖你希望根据在 VQIP 计划下进口的所有食品。你的 QAP 应作为 VQIP 申请的一部分一并提交。
我的 VQIP 质量保证计划 QAP 应包含哪些内容?
你的 VQIP QAP 应包含以下适用部分:
I. 目录(Table of Contents)
提供一份目录,列明你的 VQIP 质量保证计划 QAP 中所包含的全部信息内容。
II. 公司质量政策声明(Corporate Quality Policy Statement)
提供贵公司关于食品安全和食品安全防护、涵盖整个供应链的质量政策声明。说明该质量政策如何在企业内部向所有员工传达,以及如何向参与实施 VQIP QAP 的非申请方实体进行传达。并说明你将如何确保员工和相关非申请方实体能够接收并理解该公司的质量政策声明。
III. 组织结构与职能责任(Organizational Structure and Functional Responsibilities)
提供贵公司的组织架构图或书面说明,阐述贵公司的管理结构,包括负责实施 VQIP QAP 的人员。说明参与制定、实施和维护 VQIP QAP 的人员所承担的职能责任,并明确负责整体管理和执行 VQIP QAP 的人员姓名及职务。
同时,应明确实施 VQIP QAP 所需的非申请方实体的职能责任,并说明贵公司如何将这些职责传达给相关实体(例如通过合同)。例如,应明确外国供应商在对已在美国分销的不合规进口食品实施召回方面所承担的责任。
IV. 食品安全政策与程序(Food Safety Policies and Procedures)
提供一份书面说明(Written description),阐述你将实施的各项政策和程序,以确保食品从生产源头到进入美国过程中的食品安全(例如温控和储存控制)。请将政策和程序文件纳入你的 VQIP 质量保证计划 QAP 中,具体如下:
(1)若食品受 FSVP 或 HACCP 进口商法规的约束,且你即为 FSVP 或 HACCP 进口商,则应提供一份声明,确认你已建立相应程序,以确保遵守适用的 FSVP 或 HACCP 法规要求。
(2)若食品受 FSVP 或 HACCP 进口商法规的约束,但你并非 FSVP 或 HACCP 进口商,应提供相应程序,以确保实际的 FSVP 或 HACCP 进口商遵守适用的 FSVP 或 HACCP 相关法规要求。并举例说明程序内容,包括但不限于:
确定 FSVP 或 HACCP 进口商不受 FDA 执法行动的约束, 每年从 FSVP 或 HACCP 进口商处获得书面保证或证明(Written assurance or attestation),确认其遵守适用的 FSVP 或 HACCP 法规。
(3)提供书面程序(Written procedures),用于维持符合 FDA TPP 法规、由经 TPP 认可的认证机构签发的、外国供应商设施认证,以满足《联邦食品、药品和化妆品法案》第 806(d) 条(Section 806(d) of the FD&C Act)的要求,以及《联邦食品、药品和化妆品法案》第 801(q) 条(Section 801(q) of the FD&C Act)(21 U.S.C. 381(q))所适用的任何认证要求。
(4)提供针对每一种 VQIP 食品在运输供应链全过程中实施安全控制的程序,包括在适用情况下,符合 FDA《人用和动物用食品卫生运输法规》(Sanitary Transportation of Human and Animal Food regulation)(21 CFR part 1, subpart O)。
(5)提供用于向 FDA 及其他相关方(如非申请方实体、消费者)通报食品或外国供应商不合规情况相关信息(且该不合规对公共健康构成风险)的书面程序。应明确哪些信息仅限于组织内部沟通,以及在何种条件下需要向外国供应商或其他监管机构(如美国联邦、州和地方政府机构以及外国监管机构)进行通报。
(6)提供针对食品或外国供应商不合规(且对公共健康构成风险)的纠正措施程序,包括:对不合规食品的追溯与追踪;防止该食品进一步分销以及在必要时启动召回。同时,还应包括:与不合规外国供应商合作纠正问题的程序;停止使用某外国供应商的判定标准以及为食品寻找替代供应商的程序。
V. 食品防护政策与程序(Food Defense Policies and Procedures)
在适用情况下,提供对贵公司食品防护体系的书面说明(Written description)。应包括确保外国供应商食品防护体系符合 FDA《防止食品被故意掺假缓解策略法规》(Mitigation Strategies to Protect Food Against Intentional Adulteration regulation)(21 CFR part 121)的相关程序(如适用)。此外,还应提供对每一种 VQIP 食品在运输供应链全过程中实施安全防护控制的程序。不适用于故意掺假法规的食品,无需纳入的食品防护政策和程序。如果你的食品防护体系包括参与 CBP 的 C-TPAT(2 级或 3 级)(Level 2 or Level 3),且你已在申请中确认该参与情况,则无需就运输食品防护程序另行提供补充信息。
VI. 人员资质(Qualifications)
明确负责实施 VQIP QAP 的员工所需具备的资质要求,包括:
与《联邦食品、药品和化妆品法案》(FD&C Act)及其适用于你根据 VQIP进口的食品和外国食品供应商的实施细则相关的知识要求(例如,现行良好生产规范 CGMP、农产品安全、食品安全验证计划 FSVP、预防性控制措施、果汁 HACCP、水产品 HACCP、低酸罐头食品、故意掺假、卫生运输和食品标签),以及 各负责制定、实施和维护 QAP 的员工所需具备的资格条件(如知识、技能和培训)。
VII. QAP 的实施(QAP Implementation)
提供确保你的 VQIP QAP 保持最新并得到适当实施的程序,包括对 QAP 进行审核和更新的程序,以及在你的 VQIP 申请中提交 QAP 更新的程序。
VIII. 记录(Records)
请提供贵公司关于建立和维护与贵公司 VQIP QAP 的结构、流程、程序和实施相关的记录的书面程序。程序应明确所有与 QAP 建立和维护相关的书面记录必须清晰可读,并在 FDA 要求时予以提供。你可以使用英语以外的其他语言保存记录,但需要在合理的时间内向 FDA 提供任何被要求提供的记录的英文译本。并具体要求:
(1)QAP 的结构、流程和程序文件:
应由 QAP 计划的总体负责人签字并注明日期 应注明生效日期 应在其有效期内予以保存
(2)你为实施 QAP 计划而建立和维护的记录:
应由 QAP 中指定的责任人签字并注明日期 自创建之日起,至少应维护 2 年
IX. 定义(Definitions)
根据需要,对 VQIP QAP 中使用的术语进行定义,以便理解和实施。
X. 参考资料(References)
根据需要,提供用于制定和实施 QAP 计划的相关信息或参考资料来源。
FDA 通过这十个部分,实质上是在要求 VQIP 申请人提交一套能够证明其对进口食品在“责任分配、风险识别、过程控制、纠正机制和记录留存”等方面具备持续、系统、可审计控制能力的完整治理体系,而不仅仅是形式化文件。
应何时提交 VQIP 申请?
你可在美国东部标准时间 EST 1 月 1 日 12:00 a.m. 至 9 月 1 日 11:59 p.m. 期间提交 VQIP 申请。
VQIP 的财政年度是什么时候?
VQIP 的财政年度(Fiscal year)与美国联邦政府的财政年度一致,即每年美东时间 10 月 1 日 12:00 a.m.(EST)开始,至次年 9 月 30 日 11:59 p.m.(EST)结束。VQIP 财政年度是指经批准的 VQIP 申请人可以享受 VQIP 计划程序性便利的期间。
我是否需要每年提交新的 VQIP 申请?
是的。你必须为每一个想要参与 VQIP 的财政年度分别提交申请。但在线 VQIP 申请系统支持使用上一年度申请中的数据来填充新一年度的申请。在开始提交下一年度申请之前,如果你计划沿用当前申请中的信息,则应确保当前申请内容是最新的(即,你已提交所有适用于当前申请的修改)。在创建下一年度的新申请时,你可以新增来自新的外国供应商的新食品及其相关必要信息。
FDA 将如何审核我的 VQIP 申请?
FDA 将对你的申请进行完整性和数据准确性审查,并依据 VQIP 指南文件中列明的标准评估你是否符合 VQIP 的资格条件。FDA 将审查你在申请中列明的所有食品及外国供应商的合规历史记录,以及与每种食品的进口交易和供应链相关的所有非申请方实体的合规历史记录,包括你的申报人/报关行(Filers/brokers)。FDA 还将审查的 QAP,以评估你是否已对拟在 VQIP 计划下进口的食品在安全性和保障性方面实施了充分的控制。
如果你是 C-TPAT 计划参与方,FDA 将核实你参与 C-TPAT 计划的情况,并可能审查你的运输食品防护程序(Transportation food defense procedures)。如果你在 C-TPAT 计划中资质未达良好状态,FDA 将评估你的 C-TPAT 参与状态相关的因素是否会影响你参与 VQIP 的资格。如果你决定不再申请 C-TPAT,该决定仅在其与食品安全问题相关时才会影响你的 VQIP 资格。
如果我的 VQIP 申请未获批准,FDA 会告知原因吗?
是。在 FDA 审核你的 VQIP 申请过程中,如发现存在你可以在申请期内及时纠正的缺陷(Deficiencies),FDA 将允许你进行纠正。但如果相关缺陷未被纠正,或 FDA 另行认定你不符合参与 VQIP 的资格,FDA 将否决你的申请,并告知你被拒(Disapproval)的原因。
FDA 拒绝我的 VQIP 申请的原因有哪些?
FDA拒绝 VQIP 申请的部分原因包括但不限于:
申请材料不完整; QAP 不充分(例如,其政策和程序无法确保满足食品安全要求); 未满足一项或多项 VQIP 资格条件,且未提供合理的替代方案或说明; 提供的数据或信息不准确;或 在申请中作出虚假或欺诈性陈述。
VQIP 检查的范围和目的是什么?
FDA 可开展 VQIP 检查,以核实你是否符合 VQIP 的资格条件,并已在适用情况下全面实施了你 QAP 中所建立的食品安全和食品防护体系。VQIP 检查通常包括对书面程序(Written procedures)及证明符合 VQIP 要求的相关记录进行审查。FDA 将就任何 VQIP 检查的结果向你进行通知。
FDA 在审查我的 VQIP 申请期间,可能会要求我提交哪些额外信息?
FDA 可能要求你提交额外文件(Additional documentation)以支持你的申请。例如,如果你是 FSVP 或 HACCP 进口商,FDA 可能要求你提供 VQIP 申请中所列食品的 FSVP 危害分析文件副本,或用于满足 FSVP 或 HACCP 法规要求的实验室检测结果;如果你不是 FSVP 或 HACCP 进口商,FDA 可能要求你从该进口商处获取相关信息;FDA 还可能要求你提供申请中所列食品的标签副本,以评估是否存在与食品风险相关的标签违规(例如,未披露过敏原)。
FDA 将多久评估一次我的 VQIP 资格?
在你首次提交 VQIP 申请的年度以及之后每一年提交申请时,FDA 都将对你申请的各个方面进行审查。FDA 将审查你的检查历史记录,并可能在你首次参与 VQIP 时开展检查,以核实你的资格。此后,在你持续参与 VQIP 的情况下,FDA 至少 每 3 年 重新评估一次你的资格(Section 806(e) of the FD&C Act)。但以下情况可能促使 FDA 提前重新评估你的资格,并可能包括检查(Inspection):与你 VQIP 申请中所列食品(或类似食品)发生疫情爆发事件或召回;VQIP 食品出现新危害;你的 VQIP 申请中列明的一个或多个实体(如外国供应商、申报人/报关行)存在违规行为。此外,FDA 还将根据需要审查并评估你通过修正程序提交的申请变更。
FDA 将如何通知我 VQIP 申请已获批准(Approved)?
在 FDA 批准你的 VQIP 申请后,将向你在 VQIP 申请中提供的联系人发送电子邮件。邮件中将包含 VQIP 合规性声明 AofC 代码(Affirmation of Compliance code),该代码用于标识 VQIP 食品的报关申报。
此邮件可用于向你的业务合作伙伴证明你已参与 VQIP 计划。
你亦可通过访问 VQIP 申请系统主页(https://www.access.fda.gov/)查询你的 VQIP 申请状态。
在申请获批后,为维持参与 VQIP 的资格,我需要对我的 VQIP 申请进行哪些修改?
为了维持你在 VQIP 计划中的参与资格,并避免资格被撤销,当你采取以下任何行动时,应当及时对你的 VQIP 申请进行修正(Amend),提交相应的信息或文件:
移除在 VQIP 申请中列明、且正处于 FDA 行政或司法执法行动中的食品(例如进口预警、扣押)(Import Alert, seizure); 移除在 VQIP 申请中列明、且正处于 FDA 行政或司法执法行动中的外国供应商(例如进口预警、禁令、设施注册暂停)(Import Alert, injunction, suspension of registration); 移除某食品对应的、正处于 FDA 行政或司法执法行动中的 FSVP 或 HACCP 进口商(例如进口预警、资格取消)(Import Alert, debarment); 移除不再符合 VQIP 申报人/报关行要求的申报人/报关行; 更新你的 QAP 中与食品安全或食品防护相关的政策和程序; 提交由 TPP 认可的认证机构(CB)依据 FDA TPP 法规签发的有效设施认证(Current facility certification); 提交 FDA 要求的、用于纠正缺陷(Correct deficiencies)的相关信息或文件。
在 VQIP 财政年度内,出于业务需要,我可以对申请作出哪些修正(Amendments)?
在业务需要的情况下,你可以对 VQIP 申请进行如下修正(Amend):
新增来自已列入 VQIP 申请中的外国供应商的食品; 新增原申请中未列明的外国供应商及其食品,前提是该供应商具备由 TPP 认可的认证机构根据 FDA 的 TPP 法规签发的有效设施认证(Current facility certification); 移除(Remove)某一食品、该食品的外国供应商,或该食品对应的 FSVP 或 HACCP 进口商; 更换(Replace)已列入 VQIP 申请中的某食品的外国供应商或 FSVP / HACCP 进口商,前提是该外国供应商具备符合相关要求的有效设施认证;;以及 添加(Add)或移除申报人/报关行(Filer/broker)。
如果我对 VQIP QAP 中的食品安全或食品防护政策和程序作出了变更,却未及时在申请中更新,会有什么后果?
如果 FDA 认定你在未及时修订申请中 QAP 内容的情况下,对 QAP 的食品安全或食品防护政策和程序作出了变更,FDA 可能会根据该等变更的性质,启动撤销你参与 VQIP 资格的程序。
被撤销资格后,我如何才能恢复参与 VQIP 或获得 VQIP 程序性便利(VQIP benefits)?
如果 VQIP 的撤销是基于你不符合一项或多项 VQIP 资格条件(VQIP eligibility criteria)的证据,在你已经纠正导致撤销的相关偏差(Deviations)(问题)之后,可以在任何时间向 FDA 申请恢复你的 VQIP 参与资格及相应的 VQIP 程序性便利(VQIP benefits)。你的恢复申请应当包含相关文件,以证明你已经采取措施纠正或解决了所有导致撤销的问题。以下是你可以提交以支持恢复申请的一些示例性材料:
(1)如果你在过去 3 年内曾受到 CBP 的罚款、没收或其他制裁,你可能需要提供文件,证明你已经完成所有必要的整改,并且已与 CBP 妥善解决相关事项。
(2)如果你使用过在 FDA 不具备良好合规记录的申报人/报关行,你可能需要:
提供文件证明该申报人/报关行已接受额外培训,以确保其代表你向 FDA 提交的数据的质量有所改善; 或改用其他在 FDA 合规状态良好的申报人/报关行; 或修订你的 QAP,建立相关程序,确保今后只使用在 FDA 合规良好的申报人/报关行。
(3)如果你使用的外国供应商没有由 TPP 认可的认证机构 CB 依据 FDA 的 TPP 法规签发的有效设施认证(Current facility certification),你可能需要:将该外国供应商及其产品从你的 VQIP 申请中移除;并视需要修改 QAP,以确保你能持续维持外国供应商的有效认证状态。
(4)如果撤销是由于外国供应商存在食品安全偏差(Food safety deviation)造成的,且仅凭文件(如修订后的 SOP、HACCP 计划或批次记录)不足以证明其已充分纠正该偏差,则你可能需要重新取得该外国供应商由 TPP 认可 CB 签发的新的设施认证。
(5)如果你的 QAP 存在缺陷或内容过时,你可能需要提供相应的修订文件来纠正问题,并将更新后的 QAP 内容同步更新至你的 VQIP 申请中。
FDA 将在收到你的恢复申请后尽快进行审查。在批准恢复之前,FDA 将核实你是否已实施适当的纠正措施。FDA 可能通过实施检查(Inspection)或审查你提交的纠正措施文件来进行核实,具体方式视情况而定。如果你的 VQIP 程序性便利(VQIP benefits)未能在被撤销的同一财政年度内恢复,你可以在下一财政年度的申请期内重新提交一份新的 VQIP 申请。该申请应包含你为纠正或解决导致你资格被撤销的不合格原因而采取的措施的证明文件。
如果你的 VQIP 资格是因走私或其他欺诈行为的证据而被立即撤销(Immediately revoked),FDA 将不会恢复你参与 VQIP 的资格。
以上便是关于 FDA 自愿合格进口商计划 VQIP 的介绍。












































