【美国进口清关】FDA 医疗器械:De Novo 新分类申请
 911
911平台新政&爆款打造及差异化布局攻略揭秘,手把手教你进军巴西>>>
De Novo 新分类申请(De Novo Classification Request)是医疗器械 510(k) 和 PMA 的替代方案(Alternative)之一,适用于没有已合法上市对比器械(Legally marketed predicate device)的新型低至中等风险医疗器械,“De Novo”一词在拉丁语中意为“新”。
什么是 De Novo 新分类申请(De Novo Classification Request)
De novo 新分类流程为低风险至中等风险的新型医疗器械(Novel medical devices)提供了一条获得 I 类或 II 类重新分类的途径,前提是一般管制要求或一般管制要求和特殊管制要求能够合理保证其安全性和有效性,但目前尚无合法上市的对比器械(Predicate device)。
De Novo 分类是一个基于风险的分类过程(Risk-based classification process),通过 De Novo 新分类流程被归类为 I 类或 II 类的医疗器械可以上市销售,并可作为未来上市前通知 510(k) 申报(510(k) submissions)的对比器械(如适用)。
要向 FDA 提交 De Novo 申请,以便进行基于风险的评估,将医疗器械分类为 I 类或 II 类,有两种选择:
选项一(Option 1):
在收到针对 510(k) 申报(510(k) submission)的非实质等同 NSE(Not substantially equivalent)的判定后(即没有对比器械、不存在新的预期用途或不同的技术特性,从而引发安全性和有效性方面的不同问题) 选项二(Option 2):
申请方认定没有可作为实质等同判定依据的合法上市器械时(允许无需先提交 510(k) 即可向 FDA 提交 De Novo 申请)
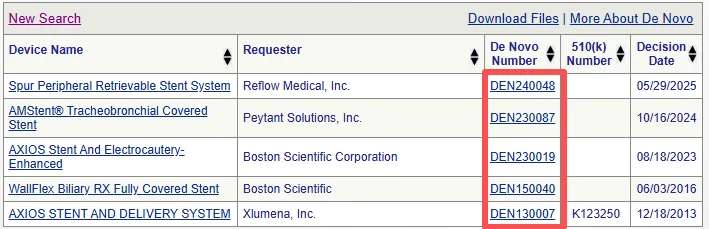
自 2025 年 10 月 1 日起,所有 De Novo 申请的提交,除非获得豁免,否则必须使用 eSTAR 以电子方式提交。若已支付相应的用户费用(User fee)且提交了有效的 eSTAR 或 eCopy,FDA 将向提交材料中指定的联系人发送确认函(Acknowledgment Letter)。申请方应会收到 FDA 的收讫确认函(Acknowledgment of receipt),其中包含分配的 De Novo 编号。De Novo 编号以“DEN”开头后接六位数字,或以“BR”开头后接六位数字。前两位数字代表收到申请的日历年份,后四位数字代表该年份的顺序申请编号。例如,2025 年收到的第一个 De Novo 申请的编号为 DEN250001 或 BR250001。
De Novo 申请 FDA 审查流程
受理性审查(Acceptance Review)(21 CFR 860.230))
在收到 De Novo 新分类申请后,FDA 将进行受理性审查。
受理性审查(Acceptance review)是一项行政性审查(Administrative review),旨在评估申请的完整性以及是否达到最低可接受标准。如果缺少任何受理要素,则应提供合理说明。
根据 21 CFR 860.230 的要求,eSTAR 系统中的受理审查已基本实现自动化,因为使用电子提交模板(Electronic submission template)正确准备的电子提交(Electronic submission)应视为完整提交。eSTAR 提交预计无需再经过重新审核 RTA(Reuse to accept)流程。但是 FDA 计划在受理审查流程中对 eSTAR 进行病毒扫描(Virus scanning)和技术筛查(Technical screening)。完整的 eSTAR 提交以及技术筛查流程的实施,均符合 21 CFR 860.230(c)(1)(i) 至 (v) 中所述的受理审查标准(Acceptance review criteria)。
技术筛查流程(Technical screening process)应在 FDA 收到 De Novo eSTAR 后的 15 个日历日内完成。FDA 仅对已支付相应用户费用的 De Novo 电子提交进行技术筛查。如果 eSTAR 提交时信息不完整, FDA 将通过电子邮件通知提交人并指出信息不完整之处,并将 De Novo 申请暂缓处理(Placed on hold)。如果在收到技术筛查缺陷通知(Technical screening deficiency notification)之日起 180 天内未收到替换的 eSTAR(Replacement eSTAR),FDA 将视 De Novo 申请为已撤销(Withdrawn),并在系统中关闭该提交。通过技术筛查的文件,其审查时限不受技术审查周期影响。对于通过技术筛查的提交(Submission),其审查时长(Review clock)从 FDA 收到提交之日起开始计算。
一旦 eSTAR 通过技术筛查且 De Novo 申请获受理后,FDA 将以电子方式通知申请方(Requester)。若 FDA 未能在受理审查期内(即收到提交后 15 个日历日内)完成技术筛查,则视为接受该 De Novo 申请进行审查,并通知申请方。
实质性审查(Substantive Review)
作为实质性审查的一部分,FDA 会对已合法上市的医疗器械类型进行分类审查(Classification review),并分析是否存在同类型的已合法上市器械。此信息用于确认该器械是否符合 De Novo 分类的条件。
在对 De Novo 申请进行实质性审查期间,FDA 可能会发现一些缺陷(Deficiencies),这些缺陷可以通过互动式审查(Interactive review)得到充分解决,而无需正式要求提供补充信息(补充信息函)(Additional Information letter)。
如果无法通过互动式审查来解决问题和缺陷(Issues and deficiencies),FDA 将向申请方(Requester)发送补充信息函(Additional Information letter)。如果发送了补充信息函,则 De Novo 申请暂缓处理(Placed on hold)。自补充信息函发出之日起申请方有 180 个日历日的时间,针对补充信息函中列明的每一项内容提交完整答复(Complete response)。
需要注意的是,FDA 必须在补充信息函发出之日起 180 个日历日内收到答复。逾期 180 日将不予延期。
若 FDA 未能在补充信息函发出之日起 180 个日历日内收到针对函中所有缺陷的完整答复,该申请将被视为撤销并从 FDA 审查系统中删除。如果 De Novo 申请(De Novo request)被删除,则 De Novo 申请方需重新提交申请以获取 FDA 对该器械的上市许可(Marketing authorization)。
申请方必须向相应的 FDA 中心(Center)提交对补充信息函的答复。答复应包括:
包括申请方名称; 标明 De Novo 编号; 标明此提交内容是对补充信息函的答复; 标明 FDA 要求提供补充信息的日期;以及 以条理清晰的方式提供所要求的信息。
最后一步是对 De Novo 申请(De Novo request)作出决定。根据 MDUFA IV 法案,FDA 的目标是在 150 个审查日(Review days)内对 De Novo 申请做出决定。审查日的计算方法是:自 FDA 收到 De Novo 申请之日起至 FDA 做出决定之日止的日历日天数,不包括因需要补充信息而暂缓处理的天数。
FDA 对 De Novo 申请的最终决定(Final Actions)
FDA 在审查 De Novo 申请后,将做出最终决定(Final decision),批准(Grant)或拒绝(Decline)该申请。在某些情况下,FDA 也会考虑撤销(Withdrawn)De Novo 申请。
批准(Grant)(21 CFR 860.260)
如果向 FDA 提供的数据和信息表明,一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)足以提供合理的安全性和有效性保证,且该器械的预期效益大于预期风险,则 FDA 将打算批准(Intends to grant)该 De Novo 申请,并为该新型器械类型制定新的分类法规(Classification regulation)。
如果 FDA 批准了 De Novo 申请:
该新型医疗器械已获准上市销售,且必须符合适用的监管控制(Regulatory controls)要求; 针对该类医疗器械制定了新的分类法规; 在适用情况下,该新型医疗器械可作为未来同类型器械的 510(k) 申报的对比器械(Predicate device); FDA 在《联邦公报》(Federal Register)上发布公告,宣布新的分类法规,以及针对 II 类医疗器械的新的特殊管制要求(New special controls); FDA 会在其网站上公布批准令副本(Copy of the granting order),通知申请方 FDA 已授予其上市许可;以及 FDA 主动生成并公开披露决策摘要(Decision summary)。
自 2010 年起,FDA 开始主动发布通过 De Novo 流程分类的医疗器械的决定摘要文件(Decision summary documents)。De Novo 决定摘要旨在客观、公正地呈现 FDA 批准 De Novo 申请所依据的科学证据。此外,对于希望将该器械作为对比器械的医疗器械制造商而言,De Novo 决定摘要还可作为参考,说明支持实质等同 SE(Substantial equivalence)所需的各类信息。这些信息可通过 De Novo 分类申请数据库(De Novo Classification Requests database)公开获取。
拒绝(Decline)(21 CFR 860.260)
通常情况下,如果出现以下情形,FDA 将拒绝 De Novo 申请:
一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)不足以合理保证该医疗器械的安全性和有效性;或 De Novo 申请中提供的数据不足以确定一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)能否合理保证该医疗器械的安全性和有效性;或 该医疗器械的预期效益不足以抵消其预期风险。
如果 De Novo 申请被拒绝,则该医疗器械属于 III 类器械,申请方不得合法上市销售该医疗器械。FDA 将向申请方(Requester)发出书面通知(Written order),说明拒绝理由,其中可能包括缺乏足以支持 De Novo 申请的性能数据。申请方通常应根据《联邦食品、药品和化妆品法案》第 515 条(Section 515 of the FD&C Act)提交上市前批准(Premarket approval)申请,或收集补充信息(Additional information)以解决相关问题,并提交包含补充信息的新的 De Novo 申请。
撤回(Withdrawal of a De Novo request)(21 CFR 860.250)
如果出现以下情况,FDA 将视为撤回(Withdrawn)De Novo 分类申请:
申请方向 FDA 提交书面通知(Written notice),声明其撤回 De Novo 申请; 申请方未能就补充信息请求提供完整答复(21 CFR 860.240),或者 FDA 指出的缺陷(Deficiencies)(21 CFR 860.230)未在 FDA 发出该请求之日起 180 天内得到解决;或 申请方未允许经授权的 FDA 雇员在合理时间内以合理方式检查设施(21 CFR 860.240),也不允许其查阅、复制及核查与 De Novo 申请相关的所有记录。
若 FDA 认定某项 De Novo 申请已被撤回,则会向申请方发出通知,并注明 De Novo 申请编号和 FDA 认定该申请撤回的日期。此类通知不会在 FDA 官网上公开发布。



























De Novo 新分类申请(De Novo Classification Request)是医疗器械 510(k) 和 PMA 的替代方案(Alternative)之一,适用于没有已合法上市对比器械(Legally marketed predicate device)的新型低至中等风险医疗器械,“De Novo”一词在拉丁语中意为“新”。
什么是 De Novo 新分类申请(De Novo Classification Request)
De novo 新分类流程为低风险至中等风险的新型医疗器械(Novel medical devices)提供了一条获得 I 类或 II 类重新分类的途径,前提是一般管制要求或一般管制要求和特殊管制要求能够合理保证其安全性和有效性,但目前尚无合法上市的对比器械(Predicate device)。
De Novo 分类是一个基于风险的分类过程(Risk-based classification process),通过 De Novo 新分类流程被归类为 I 类或 II 类的医疗器械可以上市销售,并可作为未来上市前通知 510(k) 申报(510(k) submissions)的对比器械(如适用)。
要向 FDA 提交 De Novo 申请,以便进行基于风险的评估,将医疗器械分类为 I 类或 II 类,有两种选择:
选项一(Option 1):
在收到针对 510(k) 申报(510(k) submission)的非实质等同 NSE(Not substantially equivalent)的判定后(即没有对比器械、不存在新的预期用途或不同的技术特性,从而引发安全性和有效性方面的不同问题) 选项二(Option 2):
申请方认定没有可作为实质等同判定依据的合法上市器械时(允许无需先提交 510(k) 即可向 FDA 提交 De Novo 申请)

自 2025 年 10 月 1 日起,所有 De Novo 申请的提交,除非获得豁免,否则必须使用 eSTAR 以电子方式提交。若已支付相应的用户费用(User fee)且提交了有效的 eSTAR 或 eCopy,FDA 将向提交材料中指定的联系人发送确认函(Acknowledgment Letter)。申请方应会收到 FDA 的收讫确认函(Acknowledgment of receipt),其中包含分配的 De Novo 编号。De Novo 编号以“DEN”开头后接六位数字,或以“BR”开头后接六位数字。前两位数字代表收到申请的日历年份,后四位数字代表该年份的顺序申请编号。例如,2025 年收到的第一个 De Novo 申请的编号为 DEN250001 或 BR250001。
De Novo 申请 FDA 审查流程
受理性审查(Acceptance Review)(21 CFR 860.230))
在收到 De Novo 新分类申请后,FDA 将进行受理性审查。
受理性审查(Acceptance review)是一项行政性审查(Administrative review),旨在评估申请的完整性以及是否达到最低可接受标准。如果缺少任何受理要素,则应提供合理说明。
根据 21 CFR 860.230 的要求,eSTAR 系统中的受理审查已基本实现自动化,因为使用电子提交模板(Electronic submission template)正确准备的电子提交(Electronic submission)应视为完整提交。eSTAR 提交预计无需再经过重新审核 RTA(Reuse to accept)流程。但是 FDA 计划在受理审查流程中对 eSTAR 进行病毒扫描(Virus scanning)和技术筛查(Technical screening)。完整的 eSTAR 提交以及技术筛查流程的实施,均符合 21 CFR 860.230(c)(1)(i) 至 (v) 中所述的受理审查标准(Acceptance review criteria)。
技术筛查流程(Technical screening process)应在 FDA 收到 De Novo eSTAR 后的 15 个日历日内完成。FDA 仅对已支付相应用户费用的 De Novo 电子提交进行技术筛查。如果 eSTAR 提交时信息不完整, FDA 将通过电子邮件通知提交人并指出信息不完整之处,并将 De Novo 申请暂缓处理(Placed on hold)。如果在收到技术筛查缺陷通知(Technical screening deficiency notification)之日起 180 天内未收到替换的 eSTAR(Replacement eSTAR),FDA 将视 De Novo 申请为已撤销(Withdrawn),并在系统中关闭该提交。通过技术筛查的文件,其审查时限不受技术审查周期影响。对于通过技术筛查的提交(Submission),其审查时长(Review clock)从 FDA 收到提交之日起开始计算。
一旦 eSTAR 通过技术筛查且 De Novo 申请获受理后,FDA 将以电子方式通知申请方(Requester)。若 FDA 未能在受理审查期内(即收到提交后 15 个日历日内)完成技术筛查,则视为接受该 De Novo 申请进行审查,并通知申请方。
实质性审查(Substantive Review)
作为实质性审查的一部分,FDA 会对已合法上市的医疗器械类型进行分类审查(Classification review),并分析是否存在同类型的已合法上市器械。此信息用于确认该器械是否符合 De Novo 分类的条件。
在对 De Novo 申请进行实质性审查期间,FDA 可能会发现一些缺陷(Deficiencies),这些缺陷可以通过互动式审查(Interactive review)得到充分解决,而无需正式要求提供补充信息(补充信息函)(Additional Information letter)。
如果无法通过互动式审查来解决问题和缺陷(Issues and deficiencies),FDA 将向申请方(Requester)发送补充信息函(Additional Information letter)。如果发送了补充信息函,则 De Novo 申请暂缓处理(Placed on hold)。自补充信息函发出之日起申请方有 180 个日历日的时间,针对补充信息函中列明的每一项内容提交完整答复(Complete response)。
需要注意的是,FDA 必须在补充信息函发出之日起 180 个日历日内收到答复。逾期 180 日将不予延期。
若 FDA 未能在补充信息函发出之日起 180 个日历日内收到针对函中所有缺陷的完整答复,该申请将被视为撤销并从 FDA 审查系统中删除。如果 De Novo 申请(De Novo request)被删除,则 De Novo 申请方需重新提交申请以获取 FDA 对该器械的上市许可(Marketing authorization)。
申请方必须向相应的 FDA 中心(Center)提交对补充信息函的答复。答复应包括:
包括申请方名称; 标明 De Novo 编号; 标明此提交内容是对补充信息函的答复; 标明 FDA 要求提供补充信息的日期;以及 以条理清晰的方式提供所要求的信息。
最后一步是对 De Novo 申请(De Novo request)作出决定。根据 MDUFA IV 法案,FDA 的目标是在 150 个审查日(Review days)内对 De Novo 申请做出决定。审查日的计算方法是:自 FDA 收到 De Novo 申请之日起至 FDA 做出决定之日止的日历日天数,不包括因需要补充信息而暂缓处理的天数。
FDA 对 De Novo 申请的最终决定(Final Actions)
FDA 在审查 De Novo 申请后,将做出最终决定(Final decision),批准(Grant)或拒绝(Decline)该申请。在某些情况下,FDA 也会考虑撤销(Withdrawn)De Novo 申请。
批准(Grant)(21 CFR 860.260)
如果向 FDA 提供的数据和信息表明,一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)足以提供合理的安全性和有效性保证,且该器械的预期效益大于预期风险,则 FDA 将打算批准(Intends to grant)该 De Novo 申请,并为该新型器械类型制定新的分类法规(Classification regulation)。
如果 FDA 批准了 De Novo 申请:
该新型医疗器械已获准上市销售,且必须符合适用的监管控制(Regulatory controls)要求; 针对该类医疗器械制定了新的分类法规; 在适用情况下,该新型医疗器械可作为未来同类型器械的 510(k) 申报的对比器械(Predicate device); FDA 在《联邦公报》(Federal Register)上发布公告,宣布新的分类法规,以及针对 II 类医疗器械的新的特殊管制要求(New special controls); FDA 会在其网站上公布批准令副本(Copy of the granting order),通知申请方 FDA 已授予其上市许可;以及 FDA 主动生成并公开披露决策摘要(Decision summary)。
自 2010 年起,FDA 开始主动发布通过 De Novo 流程分类的医疗器械的决定摘要文件(Decision summary documents)。De Novo 决定摘要旨在客观、公正地呈现 FDA 批准 De Novo 申请所依据的科学证据。此外,对于希望将该器械作为对比器械的医疗器械制造商而言,De Novo 决定摘要还可作为参考,说明支持实质等同 SE(Substantial equivalence)所需的各类信息。这些信息可通过 De Novo 分类申请数据库(De Novo Classification Requests database)公开获取。
拒绝(Decline)(21 CFR 860.260)
通常情况下,如果出现以下情形,FDA 将拒绝 De Novo 申请:
一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)不足以合理保证该医疗器械的安全性和有效性;或 De Novo 申请中提供的数据不足以确定一般管制要求(General controls)或一般管制要求和特殊管制要求(General and special controls)能否合理保证该医疗器械的安全性和有效性;或 该医疗器械的预期效益不足以抵消其预期风险。
如果 De Novo 申请被拒绝,则该医疗器械属于 III 类器械,申请方不得合法上市销售该医疗器械。FDA 将向申请方(Requester)发出书面通知(Written order),说明拒绝理由,其中可能包括缺乏足以支持 De Novo 申请的性能数据。申请方通常应根据《联邦食品、药品和化妆品法案》第 515 条(Section 515 of the FD&C Act)提交上市前批准(Premarket approval)申请,或收集补充信息(Additional information)以解决相关问题,并提交包含补充信息的新的 De Novo 申请。
撤回(Withdrawal of a De Novo request)(21 CFR 860.250)
如果出现以下情况,FDA 将视为撤回(Withdrawn)De Novo 分类申请:
申请方向 FDA 提交书面通知(Written notice),声明其撤回 De Novo 申请; 申请方未能就补充信息请求提供完整答复(21 CFR 860.240),或者 FDA 指出的缺陷(Deficiencies)(21 CFR 860.230)未在 FDA 发出该请求之日起 180 天内得到解决;或 申请方未允许经授权的 FDA 雇员在合理时间内以合理方式检查设施(21 CFR 860.240),也不允许其查阅、复制及核查与 De Novo 申请相关的所有记录。
若 FDA 认定某项 De Novo 申请已被撤回,则会向申请方发出通知,并注明 De Novo 申请编号和 FDA 认定该申请撤回的日期。此类通知不会在 FDA 官网上公开发布。












 热门活动
热门活动 
 其他
其他 04-16 周四
04-16 周四 热门报告
热门报告 










