【美国进口清关】FDA 监管产品:食品设施注册及常见问题解答
 1470
1470给你可复用的爆品立项与广告节奏和预算模型
根据 FD&C 法案第 415 条(21 U.S.C. 350d)规定,为在美国境内消费而从事食品(人类食品和动物食品)生产(Manufacturing)、加工(Processing)、包装(Packing)或储存(Holding)的美国国内外设施均须向 FDA 注册,特定类型的农场、零售和非营利机构可能适用于食品设施注册豁免,食品产品不需要像医疗器械那样对每个产品分别列名,但需要在设施注册时列示所涉及的食品产品类别。FDA 并不会为食品设施注册签发、盖章或邮寄任何官方证书文件。《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the Federal Food, Drug, and Cosmetic Act)[21 U.S.C. § 350d] 规定,需要向 FDA 注册的食品设施必须在每个偶数年(Even-numbered year)的 10 月 1 日至 12 月 31 日期间更新其注册。FDA 食品设施的注册信息属于保密信息(Confidential),不对外公开(Not available publicly)。
FDA 食品监管权限
进口至美国的食品(Food)、药品(Drugs)、医疗器械(Devices)和化妆品(Cosmetics)均受《联邦食品、药品和化妆品法案》(Federal Food, Drug, and Cosmetic Act)的管辖。该法案由美国卫生与公众服务部下属的食品药品监督管理局(The Food and Drug Administration of the Department of Health and Human Services)FDA 负责执行,禁止进口掺假(Adulterated)或误标(Misbranded)的物品(Articles),以及存在缺陷(Defective)、不安全(Unsafe)、不洁净(Filthy)或在不卫生条件下生产的产品。“误标”(Misbranded)包括标签中的陈述(Statements)、图案(Designs)或图片(Pictures)存在虚假或误导性,或未提供标签所要求的信息。
受 FDA 监管的进口产品在入境时须接受检查(Inspection)。不符合 FDA 法律法规要求的进口产品将被拒绝入境(Subject to refusal),此类货物(Shipments)必须进行整改、销毁或重新出口。经 FDA 酌情决定,若进口商能够使不符合规定的进口货物符合要求,则可获准进行整改。任何分拣(Sorting)、重新加工(Reprocessing)或重新贴标(Relabeling)都必须在FDA的监督下进行,费用由进口商承担。
美国食品药品监督管理局 FDA 下属的食品安全与应用营养中心 CFSAN(Center for Food Safety and Applied Nutrition)负责监管人类食品项目(Human food program)。一些受 FDA 监管的进口食品,例如糖果(Confectionery)、乳制品(Dairy products)、家禽(Poultry)、蛋类及蛋制品(Eggs and egg products)、肉类(Meats)、水果(Fruits)、坚果和蔬菜(Nuts and vegetables),也受其他机构的监管要求约束(如美国农业部)。进口食品必须纯净、有益健康、安全可食用,在卫生条件下生产,并附有信息详尽且真实的英文标签。根据美国联邦法律规定,FDA 不会也无权在进口前对任何单个食品进口商、食品产品、食品标签或具体进口批次货物进行批准、认证、许可或以其他方式给予官方认可。
只要生产、储存或以其他方式处理产品的设施(Facility)已在 FDA 注册,并且进口商已就即将入境的食品批次向 FDA 提交了事先通知 PN(Prior Notice),即可将食品进口到美国,无需事先获得 FDA 的批准。
根据 2002 年《公共卫生安全与生物恐怖主义防范和应对法案》(The Public Health Security and Bioterrorism Preparedness and Response Act of 2002),简称《生物恐怖主义法案》BTA(Bioterrorism Act)(Public Law 107-188)的规定,凡用于商业用途而进口(或拟进口)的食品,包括由个人随身携带入境的数量,均须在货物抵达美国之前,向美国食品药品监督管理局 FDA 进行规范申报(事先通知 PN)。
一般而言,如未能就 BTA 法案(Bioterrorism Act)监管的食品提交完整、及时且准确的事先通知,可能导致:
货物被拒绝入境; 货物被转移至 FDA 注册设施(费用由进口方承担); 参与进口交易的任何相关方可能承担相应的民事罚款责任(Civil monetary penalty liabilities)。
进口食品在抵达美国入境口岸时须接受美国食品药品监督管理局 FDA 的检查(Inspection)。如果发现进口食品不符合相关进口要求,FDA 有权扣留(Detain)该批货物。在美国境内,进口食品与本土生产的食品均须满足相同的法律要求。
进口时,FDA 将核实食品是否符合以下适用要求:
食品设施注册(Food facility registration)。 低酸罐头食品/酸化食品 LACF/AF(Low Acid Canned Foods/Acidified Foods)食品罐头生产企业编号 FCE(Food Canning Establishment Number)。 LACF/AF 分类识别号 SID(Schedule Identifier Number)。
此外,
美国食品药品监督管理局 FDA 会进行现场检查(Field examinations)并分析食品样品,以确保其符合适用的标准和/或标签要求。 FDA 会核查进口预警数据库(Import alert database),以确保制造商(Manufacturer)或产品不受 DWPE“无需实物检查扣留”措施的约束,并且没有被列入进口预警名单。
FDA Entry 审查员接受过培训,能够根据进口商在 Entry 报关申报文件中向 FDA 提供的信息核实产品是否符合适用要求,例如:
声明制造商 申报进口商/收货人 产品描述 合规性声明 A of C 代码
这些 Entry 申报信息将与 FDA 内部数据系统中的信息进行比对。FDA 利用内部数据系统来核实注册信息、LACF/AF 流程备案(如适用)或其他产品要求,并确定企业/产品是否受 DWPE 约束。如果提交的信息匹配,则视为合规;如果提交的信息不匹配,FDA 可能会收集更多信息或扣留该产品。
据 FDA 介绍,提交正确准确的 Entry 数据以及相关的 A of C 代码将有助于加快报关 Entry 审核流程。准确提供这些信息可以提高你的货物通过电子方式处理而非被 HOLD 扣留进行人工审核的可能性,因为 FDA 的进口筛查工具 PREDICT 可以将申报信息与 FDA 的内部数据系统进行比对。
食品合规性声明代码 A of C(Affirmation of Compliance codes)是一个三字母代码,可在进口时提供,以协助 FDA 审查。FDA 使用 A of C 代码来协助核实你的产品是否符合相关要求。提供正确的 A of C 代码可以降低你的货物在 FDA 进口筛查过程中被扣留进行进一步 Entry 审查的可能性。提交 A of C 代码仅在某些情况下是强制性的,并非所有情况都需要提交。除了所有强制性 A of C 代码外,提交自愿性 A of C 代码可能有助于加快你的货物报关 Entry 的初步筛查和审查。
FDA 食品设施注册(Food Facility Registration)
《2002 年公共卫生安全与生物恐怖主义防范及应对法案》(Public Health Security and Bioterrorism Preparedness and Response Act of 2002)(生物恐怖主义法案)BTA(Bioterrorism Act)(Pub. L. 107-188)于 2003 年 12 月 12 日实施,所有进口到或拟进口到美国的食品,无论是供人类还是动物食用,都必须遵守该法案的要求。BTA 法案指示美国卫生与公众服务部下属的食品药品监督管理局 FDA,作为食品监管机构,采取措施保护公众免受针对美国食品供应链的潜在或实际恐怖袭击及其他与食品相关的紧急事件的威胁。
为了执行 Bioterrorism Act 法案的某些条款(Provisions),美国食品药品监督管理局 FDA 制定了相关法规(Regulations),要求:
食品设施(Food facilities)必须向 FDA 注册,并且 进口食品在抵达美国之前必须提前通知 FDA(食品进口事先通知 PN(Prior notification))。
这些法规于 2003 年 12 月 12 日生效。

2011 年,时任美国总统奥巴马签署了 FDA《食品安全现代化法案》FSMA(Food Safety Modernization Act)(Pub. L. 111-353),该法案通过强化食品安全体系,使 FDA 能够更有效地保障公众健康。它赋予 FDA 新的工具和权限,以确保进口食品(包括人类和动物食品)符合与美国本土生产的食品相同的安全标准。《FDA 食品安全现代化法案》FSMA(Food Safety Modernization Act)对《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the Federal Food, Drug, and Cosmetic Act)[21 U.S.C. § 350d](FDA 食品设施注册的法律基础条款)的相关部分进行了修订,新条款要求为在美国境内消费而从事食品(人类食品和动物食品)生产(Manufacturing)、加工(Processing)、包装(Packing)或储存(Holding)的设施(Facilities)(包括美国境外食品设施)向 FDA 提交额外的注册信息(除非符合可以豁免的情况,参见 21 CFR 1.226),其中包括一项保证(Assurance),确认 FDA 可以在 FD&C 法案允许的时间和方式下对该设施进行检查(Inspect)。经 FSMA 修订的 FD&C 法案第 415 条(Section 415 of the FD&C Act)还要求所有依法需要向 FDA 注册的食品设施必须每两年更新一次注册,并赋予 FDA 在特定情况下暂停食品设施注册的权限。具体而言,如果 FDA 认定已注册的食品设施生产、加工、包装、接收或储存的食品存在合理可能性(Reasonable probability)会对人类或动物造成严重的健康危害或死亡,FDA 可以下令暂停(Suspend)该设施的注册资格,若该设施:
1,造成、导致或以其他方式对这种合理可能性负有责任;或
2,明知或有理由知道这种合理可能性;仍对相关食品进行包装、接收或储存。
一旦食品设施的 FDA 注册被暂停,则该设施的食品产品将被拒绝进口至美国市场。
向 FDA 进行食品设施注册不需要任何费用(21 C.F.R. 1.231(c))。自 2020 年 1 月 4 日起,注册人必须以电子方式向 FDA 提交注册、注册续期、更新注册或注销注册,除非 FDA 根据 21 CFR 1.245 授予豁免(参见 21 CFR 1.231(a)(2) 和 (b)、1.234(d) 和 1.235(d))。需要向 FDA 进行注册的食品设施(Food facilities)可以通过 FDA 行业系统 FIS(FDA Industry Systems):https://www.access.fda.gov/ 以电子方式直接在线进行食品设施(Food facility)注册、更新注册或注销注册(或授权其他人代为操作)。
根据《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the Federal Food, Drug, and Cosmetic act)规定,贸易商/经销商(Traders/brokers)不需要注册。另外,位于美国境外的食品设施注册还必须指定一名美国代理。
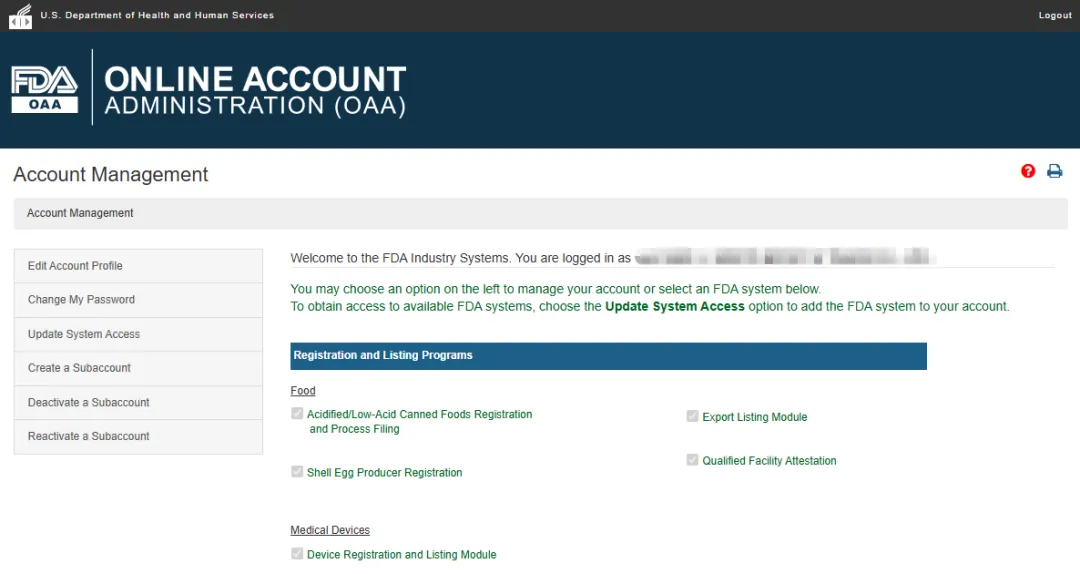
登录 FIS 系统后,可以为你的 FIS 帐户(FIS Account)添加系统/模块访问权限(Add System/Module Access),点击系统主页左侧账户管理下的“更新系统访问权限”,勾选你想要访问的系统旁边的方框,然后点击“提交”添加。
要开始食品设施注册,从 FIS 账户管理主页(Account Management Home Page)的可用系统列表中选择“FURLS 食品设施注册模块”FFRM(FURLS Food Facility Registration Module)。FDA 食品设施注册需提供以下信息:
注册类型(Type of Registration) 设施名称/地址信息(Facility Name / Address Information) 首选邮寄地址信息(可选)(Preferred Mailing Address Information (Optional)) 总公司名称/地址信息(Parent Company Name/Address Information) 设施紧急联系信息(Facility Emergency Contact Information) 经营名称(Trade Names):根据《联邦法规汇编》第 21 编第 1.227 条(21 CFR 1.227),“经营名称”(Trade name)是指食品设施开展业务时所使用的名称,而“品牌名称”(Brand name)则是与具体产品相关联的名称。根据 21 CFR 1.232(a)(5),负责提交食品设施注册的主体必须在注册信息中列明该设施开展业务所使用的所有经营名称。食品设施注册并不要求列出该设施所生产、加工、包装或储存的所有产品品牌名称。 美国代理(United States Agent) 季节性设施运营日期(可选)(Seasonal Facility Dates of Operation (Optional)) 一般产品类别 – 人用食品/动物食品/两者兼有(General Product Categories – Human/Animal/Both) 一般产品类别 – 供人类食用的食品;以及设施内开展的活动类型(General Product Categories – Food for Human Consumption; and Type of Activity Conducted at the Facility) 一般产品类别 – 供动物食用的食品;以及设施内开展的活动类型(General Product Categories – Food for Animal Consumption; and Type of Activity Conducted at the Facility) 所有者、经营者或负责人信息(Owner, Operator, or Agent in Charge Information) 检查声明(Inspection Statement):确认 FDA 可以依据 FD&C 法案的规定,在合适的时间、以合适的方式对设施进行检查 认证声明(Certification Statement):声明所提交的信息真实准确,且提交人已获得授权
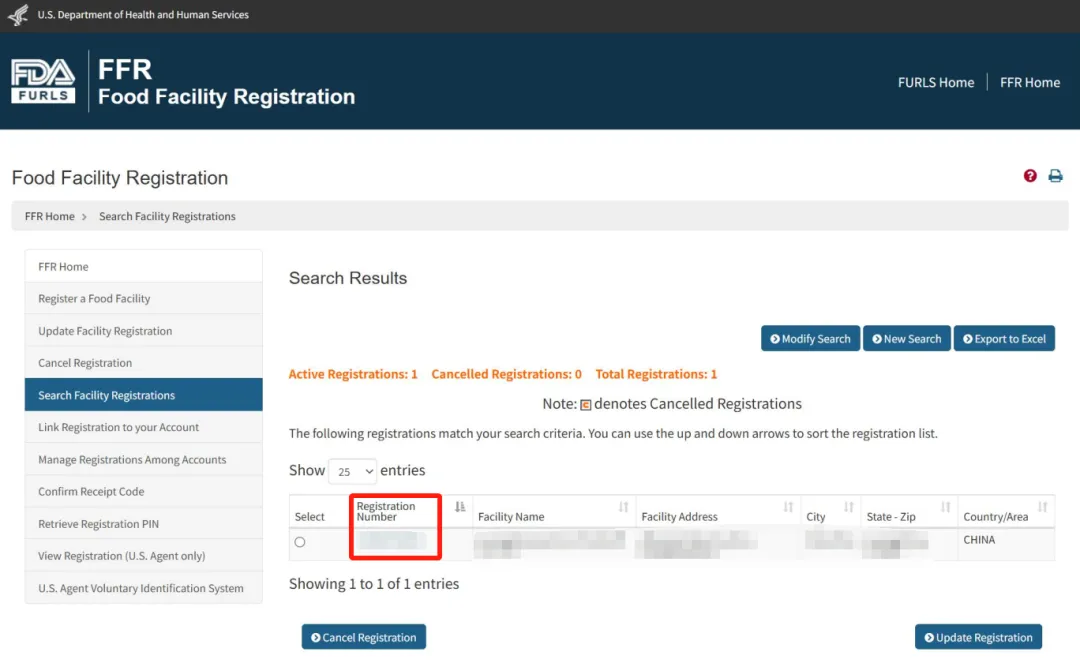
完成注册后,FDA 将为成功注册的食品设施分配一个注册号(Registration number)。但 FDA 不颁发注册证书(Certificate of registration)或产品状态证明(Product status)(如低酸罐头食品)(Low acid canned food),亦不认可任何私人公司(Private business)颁发的注册证书或产品状态证明,FBA 告知其 Logo 标识仅供 FDA 官方使用,不得用于私营企业的任何材料。
FDA 食品设施注册常见问题解答
为什么食品设施需要向美国食品药品监督管理局 FDA 进行注册?
食品设施注册 FFR(Food facility registration)有助于美国食品药品监督管理局 FDA 确定潜在生物恐怖主义(Bioterrorism)时间或食源性疾病暴发(Foodborne illness outbreak)事件的发生地点和来源,并有助于该机构快速通知可能受影响的设施。食品设施注册要求最初源于 2002 年的《公共卫生安全和生物恐怖主义防范与应对法案》(The Public Health Security and Bioterrorism Preparedness and Response Act of 2002),该法案修订了《联邦食品、药品和化妆品法案》(Federal Food, Drug, and Cosmetic Act),要求为在美国境内消费而从事食品(人类食品和动物食品)生产(Manufacturing)、加工(Processing)、包装(Packing)或储存(Holding)的设施(Facilities)(包括美国境外食品设施)向 FDA 注册。
随后,《FDA 食品安全现代化法案》FSMA(The FDA Food Safety Modernization Act)再次修订了 FD&C 法案(FD&C Act),要求美国境内外食品设施向 FDA 提交某些新增信息,并每两年更新一次注册。2016 年,FDA 发布了一项最终规则,更新了 FDA 的食品设施注册法规,其中包括反映 FSMA 修订内容的条款。
哪些食品设施必须向美国食品药品监督管理局 FDA 进行注册?
如果你是为在美国境内消费而从事食品(人类食品和动物食品)生产(Manufacturing)、加工(Processing)、包装(Packing)或储存(Holding)的设施(Facilities)(包括美国境外食品设施)的所有者(Owner)、经营者(Operator)或负责人(Agent),则必须向 FDA 注册,除非符合豁免条件。
哪些食品设施可免于注册要求?
符合以下定义的机构(Establishments)无需进行食品设施注册:初级生产农场(Primary production farm)、从事二次活动的农场(Secondary activities farm)、零售食品机构(Retail food establishment)、餐馆(Restaurant),或非营利性食品机构(Nonprofit food establishment)。上述定义可参见 21 CFR 1.227。
此外,某些其他实体亦无需注册,包括但不限于:某些渔船(Fishing vessels);境外食品设施,若该设施生产的食品在进入美国之前,在美国境外由另一家设施进一步制造或加工;以及根据特定法规,由美国农业部 USDA 对整个设施进行全面监管的设施。关于无需注册的设施类型,可参见 21 CFR 1.226。
然而,混合类型设施(Mixed-type facilities)必须进行注册。混合类型设施是指同时从事注册要求所豁免的活动与需注册的活动的设施。其中一个例子是 “农场混合类型设施”(Farm mixed-type facility),即该机构本身属于农场,但同时从事了超出“农场”定义范围、因而需要注册的活动。
请注意,FDA 计划启动一项可能修改“农场”(Farm)定义的立法规则制定程序。该规则制定可能会使某些目前被认定为需要注册的设施转而被认定为农场。FDA 并不预计该规则制定会导致任何当前被认定为“农场”(Farm)的主体被重新认定为“设施”(Facility)。然而,在该规则制定正式完成之前,凡属于美国境内或境外食品设施的主体,仍须履行食品设施注册义务,并且每两年更新一次注册。
食品设施何时需要更新注册?
食品设施必须每两年更新一次注册,更新期为每个偶数年(Even-number year)的 10 月 1 日至 12 月 31 日。
如果食品设施未按要求更新注册,FDA 将视其注册失效。
食品设施注册是否包含允许 FDA 检查该设施的保证(Assurance)?
是的。无论美国境内外食品设施的注册,均包含允许 FDA 根据《联邦食品、药品和化妆品法案》(FD&C Act)授权的时间和方式进行检查(Inspect)的保证。
设施注册是否需要支付费用?
不需要。初始注册、更新注册信息、续期注册或注销注册均不收取任何费用。
根据食品设施注册要求,何时必须进行首次注册?
若你需向 FDA 注册,则必须在设施开始进行食品生产/加工、包装或储存操作之前完成注册。
需要向 FDA 注册的设施何时需要向 FDA 提交注册续期申请(Registration renewal)?
《联邦食品、药品和化妆品法案》第 415(a)(3) 条(Section 415(a)(3) of the FD&C Act)规定,需要向 FDA 注册的设施必须每两年更新一次注册,更新期为每个偶数年的 10 月 1 日至 12 月 31 日。
若食品设施未按要求续期注册,FDA 将视其注册失效(21 CFR 1.241(b))。
如何通过电子方式提交注册或注册续期申请?
你或你授权的个人可通过 FURLS 食品设施注册模块 FFRM(Food Facility Registration Module)以电子方式在线提交设施注册或注册续期(Registration renewal)申请,网址为https://www.access.fda.gov。你需要 FDA 行业系统 FIS(FDA Industry Systems)账户 ID 和密码才能访问该电子系统。
你也可以使用该电子系统更新你的注册信息或提交注销注册申请(例如,由于所有权变更或停业)。
如何通过邮寄或传真方式提交注册或注册续期申请?
自 2020 年 1 月 4 日起,注册人必须以电子方式向 FDA 提交注册或注册续期申请,除非 FDA 已根据《联邦法规汇编》第 21 篇第 1.245 条(21 CFR 1.245)(参见 21 CFR 1.231)授予豁免。如果 FDA 已根据 21 CFR 1.245 授予豁免,注册人(Registrant)可以通过邮寄或传真方式进行注册或续期。如果通过邮寄或传真方式提交注册或注册续期申请,则必须使用纸质版的 FDA 3537 表格(Form FDA 3537)。
食品设施注册需要提交哪些信息?
根据 21 CFR 1.232 的规定,美国国内外食品设施注册需要提供以下信息:
设施名称、地址、电话号码和紧急联系电话; 首选邮寄地址(如与机构地址不同); 总公司名称、地址和电话号码(如果该设施是总公司的子公司); 该设施使用的所有商业名称(Trade names); 所有者、经营者或负责人(Agent)的姓名、地址和电话号码; 所有者、经营者或负责人(Agent)的电子邮件地址(除非 FDA 根据 21 CFR 1.245 授予豁免); 在该设施内生产/加工、包装或储存的任何食品适用的食品产品类别,如 FDA 3537 表格中所述; 根据 21 CFR 1.232(a)(8) 的规定,该设施针对每种食品类别开展的活动类型; 所有者、经营者或负责人(Agent)出具的声明(Statement),承诺允许 FDA 在《联邦食品、药品和化妆品法案》允许的时间和方式下对该设施进行检查(Inspect); 所有者、经营者或负责人(Agent)出具的声明(Statement),确认所提交信息真实准确。如果提交表格的个人(Individual)并非设施的所有者、经营者或负责人(Agent),则注册信息还必须包含一份该个人签署的声明,确认所提交的信息真实准确,并证明其已获得授权提交注册,同时须提供授权提交注册的个人的姓名、地址和电话号码。此外,除非 FDA 已根据 21 CFR 1.245 授予豁免,否则注册信息必须包含授权提交注册的个人的电子邮件地址。
此外,自 2020 年 10 月 1 日起,食品设施注册必须提交经 FDA 认可的唯一设施标识符 UFI,该 UFI 须与注册信息一同提交(21 CFR 1.232(a)(2))。每份注册申请必须包含申请人的姓名。如选择通过纸质方式提交时,则还必须包含申请人的签名(21 CFR 1.230)。
对于美国境内设施(Domestic facility),注册信息还必须包括:
该设施联系人的电子邮件地址; 紧急联系人电话号码及电子邮件地址(若与联系人电子邮件地址不同)。
对于美国境外设施(Foreign facility),注册信息还必须包括:
外国设施在美国的代理(U.S. agent)的姓名、完整地址、电话号码和电子邮件地址; 紧急联系人电话号码和电子邮件地址。
哪些 UFI 被 FDA 认可用于食品设施注册?
提交唯一设施标识符 UFI(Unique Facility Identifier)的要求于 2020 年 10 月 1 日生效。
目前,FDA 认可数据通用编号系统(Data Universal Numbering System)DUNS 编号作为可接受的 UFI。
如何获得 FDA 认可的 UFI?
目前,DUNS 编号是 FDA 认可的食品设施注册(Food facility registration)首选唯一设施标识符 UFI。DUNS 编号由邓白氏公司(Dun & Bradstreet)分配和管理,可免费获取。
我是否需要在食品设施注册申请中提供食品类别信息?
是。你的食品设施注册必须包含你在该设施内生产/加工、包装或储存的任何食品所适用的食品类别,如 FDA 3537 表格(Form FDA 3537)(21 CFR 1.232(a)(7))所示。
食品设施注册编号(Registration number)何时分配 ?
FDA 会分配一个注册编号,以确认食品设施已注册。只有在 FDA 核实注册信息中的特定内容后,才能确认企业的注册。具体而言,FDA 只有在核实设施的 UFI 及设施具体地址、确认指定的美国代理同意担任注册设施的美国代理(针对美国境外设施注册)以及确认并非由所有者、经营者或负责人提交的注册申请确实已获得授权人正式授权后,才会确认注册(参见 21 CFR 1.231)。成功核实上述信息后,FDA 将分配注册号,并通过电子邮件或美国邮政信函通知注册人该设施的注册编号(Registration number)和 PIN 码(PIN number)。
注册号的分配意味着什么?
注册号的分配意味着该食品设施已在 FDA 完成注册。但注册号的分配并不意味着 FDA 对该设施或其产品给予任何形式的批准或认可(Approval or endorsement)。
食品设施注册信息或与此类注册信息相关的信息(如已注册设施列表)是否向公众公开?
《联邦食品、药品和化妆品法案》第 415(a)(5) 条(Section 415(a)(5) of the FD&C Act)规定,根据《联邦法规汇编》第 21 编第 1 部分 H 子部分提交的注册设施列表及注册文件(包括这些文件中提供的信息)不受《信息自由法案》FOIA(Freedom of Information Act)(5 U.S.C. 552)的公开约束。此外,任何从该注册列表或注册文件中获取的、能够披露特定注册人身份或位置的信息,也不受 5 U.S.C. 552 的披露要求的约束。
FDA 是否要求在食品标签上显示食品设施注册号?
否。食品标签上无需标注与食品生产加工、包装或储存相关的设施的注册编号。FDA 实际上并不鼓励食品设施在食品标签上标注其注册编号,以防止他人将注册编号用于不当目的。
FDA 是否可以暂停(Suspend)食品设施的注册?
是。《联邦食品、药品和化妆品法案》第 415(b) 条(经 FSMA 修订)赋予 FDA 通过行政命令暂停依据第 415 条注册的设施注册资格的权力。
FDA 在什么情况下可以暂停(Suspend)根据《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the FD&C Act)注册的设施的注册?
自 2011 年 7 月 3 日起,注册设施开始受到《联邦食品、药品和化妆品法案》第 415(b) 条(Section 415(b) of the Federal Food Drug and Cosmetic Act)规定的注册暂停条款(Suspension of registration provisions)的约束。
当出现以下情况时,美国食品药品监督管理局 FDA 可下令暂停食品设施的注册:
1,FDA 认定,由该注册设施生产、加工、包装、接收或储存的食品存在对人类或动物造成严重的不良健康后果或死亡(SAHCODHA)的合理可能性(Reasonable probability);
2,该设施:
a, 造成、导致或以其他方式对 SAHCODHA 的合理可能性负有责任;或
b, 明知或有理由知道存在 SAHCODHA 的合理可能性;仍对相关食品进行包装、接收或储存(Section 415(b) of the FD&C Act)。
食品设施的注册被 FDA 暂停后会有什么影响?
若某个设施的注册被暂停,任何人不得从该设施向美国进口或出口食品,不得提议从该设施向美国进口或出口食品,也不得以其他方式将该设施的食品引入美国州际或州内贸易(参见 《联邦食品、药品和化妆品法》第 415(b)(4) 条)(Section 415(b)(4) of the FD&C Act)。
根据《联邦食品、药品和化妆品法案》第 415 条已向 FDA 注册的食品设施是否需要续期更新注册?
是。根据《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the FD&C Act )规定,所有需向美国食品药品监督管理局 FDA 注册的食品设施都必须每两年向 FDA 更新一次注册,续展期为每个偶数年的 10 月 1 日至 12 月 31 日。
食品设施何时需要注册或更新注册(Renew registration)?
凡为在美国境内消费而从事食品生产(Manufacturing)、加工(Processing)、包装(Packing)或储存(Holding)的设施(Facilities)(包括美国境外食品设施)的所有者、经营者或负责人(Agent),必须在开始此类活动前向 FDA 进行注册。注册有效期为 2 年,续展期为每个偶数年的 10 月 1 日至 12 月 31 日。
已注册的境外食品设施是否需要续展更新注册?
是。根据 FDA《食品安全现代化法案》FSMA,所有根据《联邦食品、药品和化妆品法案》第 415 条(Section 415 of the FD&C Act )规定需要向 FDA 注册的食品设施,包括美国境外食品设施,都必须在注册续期期间向 FDA 提交更新注册。
如何完成食品设施注册?
自 2020 年 1 月 4 日起,除非获得 FDA 的豁免,否则所有设施注册、注册续期、注册更新和注销注册都必须通过电子方式向 FDA 提交。如需获得豁免,注册人必须向 FDA 提交书面申请(Written request),阐明为何无法合理使用电子注册系统(例如,无法访问互联网)。获得豁免的设施可以通过邮件或传真提交设施注册申请。
我的注册信息现在有变更,我必须现在提交更新吗?还是可以等到下一次两年一次的注册更新期再一起修改?
根据 21 CFR 1.232 的规定,食品设施的所有者、经营者或负责人,必须在任何已提交的必要注册信息发生变更后的 60 个日历日内,向 FDA 提交注册信息更新,但设施所有者变更的情况除外(21 CFR 1.234(a))。如果设施的所有者发生变更,原所有者必须在变更发生后的 60 个日历日内取消该设施的注册,而新所有者必须重新为该设施进行注册(21 CFR 1.234(b))。如果设施先前提交的的必要注册信息在下一个两年一次的注册更新期开始之前或期间内发生变化,注册人可以选择将该变更信息作为年度注册更新的一部分一并提交,前提是该更新仍需在变化发生后的 60 个日历日内完成提交。需要注意的是,即使设施在下一个两年一次的更新期开始之前已经向 FDA 单独提交了注册信息更新,该设施仍必须在两年一次的注册更新期内完成注册更新。
食品设施(Food facility)是否必须通过第三方注册机构(Third-party registrar)进行初始注册、更新注册信息、续期注册或注销注册?
否。FDA 并不要求食品设施(Food facility)必须通过第三方注册机构向 FDA 提交初始注册、更新注册信息、续期注册或注销注册。
食品设施的所有者、经营者或负责人必须自行完成初始注册、更新注册信息、续期注册或注销注册(参见 Section 415(a) of the FD&C Act 和 21 CFR 1.225, 1.234)。食品设施的所有者、经营者或负责人可以授权他人代表其进行食品设施注册、更新或注销(因所有权变更导致的注销除外)(21 CFR 1.225, 1.234)。被授权的个人(Individual)可以是(但非必须)外国设施的美国代理(U.S. agent)。
若食品设施未进行注册,会发生什么情况?
根据《联邦法规汇编》第 21 编第 1 部分 H 子部分(21 CFR Part 1, Subpart H)的规定,未完成食品设施设施、更新所需信息或取消注册均属违反《联邦食品、药品和化妆品法案》的行为(参见 21 C.F.R. 1.241)。如果外国食品设施(Foreign food facility)需要向美国食品药品监督管理局 FDA 注册但未履行义务完成注册,则该设施生产的、正在进口或拟进口至美国的食品将根据《联邦食品、药品和化妆品法案》第 801(l) 条(Section 801(l) of the FD&C Act)的规定被拒绝入境(Subject to refusal)。
食品设施在两年一次的更新注册流程中 FDA 会分配新的注册号吗?
否。食品设施根据两年一次的更新注册流程进行设施注册更新时,不会获得新的设施注册号。
FDA 如何核实食品设施的注册情况?
对于需要进行食品设施注册(Food facility registration)的公司(Firms),FDA 将核实其注册信息。FDA 会将提交的信息与 FDA 的内部数据系统进行比对。如果信息匹配,则视为合规;如果信息不匹配,FDA 可能需要收集补充信息(Additional information),或扣留(Detain)相关产品。












































