【美国进口清关】FDA 合规性声明代码(A of C)
 1403
1403给你可复用的爆品立项与广告节奏和预算模型
合规性声明代码(A of C)(Affirmation of Compliance codes)是一个三字母代码(如 COS、DEV、FCE、LST、DUN 等),通常后面再补充具体的限定符(编号信息)(如注册编号、列名编号、批准编号等),可在进口时提供以协助 FDA 审查。FDA 使用 A of C 代码来协助核实你的产品是否符合相关要求。
FDA 监管产品进口流程(Import Process)
1993 年美国海关现代化法案(Mod Act 法案)最重要的影响之一,是明确规定各方在向美国进口货物时必须采取合理谨慎的措施(Exercise reasonable care)。经修订的《关税法案》第 484 条(Section 484 of the Tariff Act, as amended)要求备案进口商在进口申报(Make entry)时须尽合理谨慎义务,提交任何必要的信息以便美国海关和边境保护局 CBP 确定商品是否可以放行;并采取合理谨慎的措施,向 CBP 提交申报价值(Declared value)、商品分类(Classification)和税率(Rate of duty)以及其他必要的文件或信息,以便 CBP 正确评估关税、收集准确的统计数据并确定是否满足任何其他适用法律要求,从而完成进口申报。
Mod Act 法案从根本上改变了进口商与 CBP 之间的关系,将申报进口商品价值、分类和适用关税税率的法律责任转移至进口商。“知悉合规”(Informed Compliance)的核心之一在于 CBP 与进口商的责任共担:即 CBP 将其要求告知进口商,而进口商则应采取合理的谨慎措施(Reasonable care),确保向 CBP 提供准确、及时的进口相关数据。
所有进口至美国的受 FDA 监管的产品必须同时满足美国海关和边境保护局 CBP 和美国食品药品监督管理局 FDA 的监管要求(Regulatory requirements)。不符合 FDA 监管要求的产品在入境时可能被扣留(May be detained upon entry)。
CBP 负责执行经修订的《1930 年关税法案》(Tariff Act of 1930 as amended)。其主要职责包括:评估和征收进口商品的所有关税、税款和费用;管理并审核进口报关单(Import entry forms);执行 CBP 相关法律;以及执行某些航行法律和条约(Navigation laws and treaties)。FDA 与 CBP 就《食品、药品和化妆品法案》第 801 条(《美国法典》第 21 编第 381 条)(Section 801, Title 21 U.S.C. 381)达成合作执法协议。
向 CBP 提交的受 FDA 监管产品的 Entry,也将以电子方式提交给 FDA 进行审核。进口商或报关行必须通过自动化商业环境 ACE 系统向 CBP 提交所需的进口申报信息(Required entry information)。
美国食品药品监督管理局 FDA 对 CBP 的 ABI/ACE 系统申报 Entry 的电子筛查要求申报人提供以下补充信息(Additional information):
FDA 产品代码(FDA product code) 外国制造商(Foreign manufacturer)的 MID 代码(美国海关使用 MID 作为制造商识别码) 外国发货人(Foreign shipper)的 MID 信息,包括城市和国家,可能与外国制造商相同,也可能不同 原产地(Country of origin) 适用的合规性声明代码(Applicable affirmations of compliance codes) 进口报关单中所述商品的协调关税表(HTS)编码
HTS 编码(HTS code)是一种分类代码(Classification code),用于为进口到美国的商品提供适用的关税税率(Tariff rates)和统计类别(Statistical categories)。

FDA 强制性产品数据(Mandatory product data)申报
进口商可在提交申报时提供准确完整的信息,并在收到补充材料要求后及时回应,从而加快 Entry 审查流程(Entry review process)。
什么是 A of C 代码(Affirmation of Compliance Codes)
所有受 FDA 监管的产品在申报入境时均须符合相关规定。
为协助加快 FDA 对产品合规性(Product compliance)的审查,申报人(Entry filer)可在申报时提交补充信息,例如注册编号、列名编号和批准编号。这些信息可通过合规性声明代码(Affirmation of Compliance codes)(A of C codes)提交。
通过使用 A of C 代码(A of C code),申报人确认在 FDA 申报行项(FDA line)中列明的企业和/或产品符合各代码的具体要求。即主动向 FDA 声明某批货物符合特定 FDA 要求,并提供相关证书/文件编号,让 FDA 自动比对核验。
根据进口产品的不同,提交 A of C 代码仅在特定情况下强制要求,并非所有情况都需要提交。除了所有强制性 A of C 代码(Mandatory A of C codes)外,提交自愿性 A of C 代码(Voluntary A of C codes)可能有助于加快你的 Entry 初步筛查和审查流程(Initial screening and review),降低你的货物(Shipment)在 FDA 进口筛查过程(Import screening process)中被扣留(Held)进行进一步 Entry 审查(Entry review)的可能性。
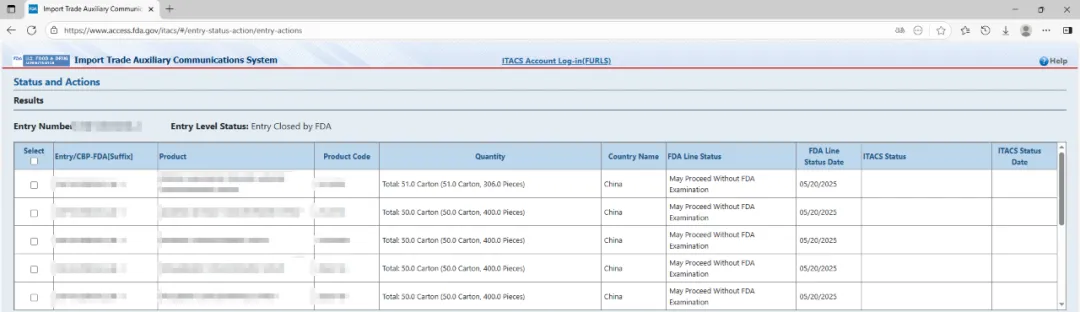
在收到准确完整的合规性声明信息后,FDA 的自动化风险评估系统 PREDICT 将根据内部数据库验证信息,能快速地对未因其他任何筛查标准(Screening criteria)而被扣留的低风险货物(Low-risk shipments)发出“自动放行”(May Proceed)指令。如果自动查找失败,则该 Entry line 将被转发(Forwarded to)给 FDA 的 Entry 审核人员(Entry reviewer)进行人工处理(Manual processing)。
什么是 A of C 代码限定符(Qualifier)?
A of C 代码限定符提供产品和制造商的特定信息。FDA 使用这些信息来验证产品是否符合规定。某些合规性声明代码需要提供产品制造商的注册编号(Registration number)(每个设施的注册号是唯一的)或产品批准编号(Approval number)(每个产品的批准编号是唯一的)。
常见的一些 A of C 合规性声明代码定义及示例
COS 化妆品注册号(Cosmetic Registration Number)
此项合规性声明代码及其限定符信息应为对应申报 FDA 行项(FDA line)中产品的化妆品注册号。
示例:COS 1061499
COS 1234567890
DDM 医疗器械国内制造商(Device Domestic Manufacturer)
此项合规性声明代码及其限定符信息应为对应申报 FDA 行项(FDA line)中产品的美国国内制造商的 FDA/CDRH 医疗器械注册号
示例:DDM 3003999999
DEV 医疗器械外国制造商注册号(Device Foreign Manufacturer Registration Number)
此项合规性声明代码及其限定符信息应为对应申报 FDA 行项(FDA line)中产品的外国制造商的 FDA/CDRH 医疗器械注册号
示例:DEV 3003999999
DEV 9699123
FAP 食品添加剂申请批准编号(Food Additive Petition Approval Number)
此合规性声明代码仅适用于进口纯食品添加剂用于食品生产过程的情况。其限定符信息应为对应申报 FDA 行项(FDA line)中产品的食品添加剂申请批准编号。
示例:FAP 123456
FCE 食品罐头生产企业编号(Food Canning Establishment Number)
此合规性声明代码用于识别酸性和/或低酸性罐头食品的生产商。其限定符信息应为对应申报 FDA 行项(FDA line)中产品的食品罐头生产企业编号。
示例:FCE 12345
IFR 进口商食品设施注册编号(Importers Food Facility Registration Number)
此确认标识可用于食品进口商。
示例:IFR 12345678901
LST 医疗器械列名编号(Device Listing Number)
此项合规性声明代码及其限定符信息应为对应申报 FDA 行项(FDA line)中产品的医疗器械列名编号。
示例:LST E199100












































