【美国进口清关】进口食品 FDA 事先通知 PN 及常见问题解答
 1510
1510给你可复用的爆品立项与广告节奏和预算模型
2002 年的 BTA 法案要求自 2003 年 12 月 12 日起,任何受美国食品药品监督管理局 FDA 监管的供人类和其他动物食用的食品进口至美国之前,都必须向 FDA 提交事先通知 PN,除非该食品符合豁免条件。PN 使 FDA 有时间在受其监管的食品进入美国之前审查和评估相关信息,并对受污染食品进行检查和拦截。FDA 将利用事先通知中提供的信息来决定是否对抵达美国的食品进行检查(Inspect)或抽样(Sample),PN 通知内容包含产品信息、数量、包装规格以及相关设施信息,例如制造商、发货人、所有者和最终收货人等主体信息。未经充分事先通知而进口或拟进口至美国的食品将被拒绝入境。
进口食品 FDA 事先通知要求背景
《2002 年公共卫生安全和生物恐怖主义防范和应对法案》(The Public Health Security and Bioterrorism Preparedness and Response Act of 2002)(简称《生物恐怖主义法案》)(Bioterrorism Act)要求美国卫生与公众服务部下属的美国食品药品监督管理局 FDA,作为食品监管机构,采取额外措施保护公众免受针对美国食品供应链的潜在或实际恐怖袭击,以及应对其他与食品相关的紧急事件。
Bioterrorism Act 法案于 2002 年 6 月 12 日签署生效。除其他内容外,该法案通过增设第 801(m) 条(Section 801(m))对《联邦食品、药品和化妆品法案》(FD&C Act)进行了修订(Amended),要求进口食品在抵达美国前必须向美国食品药品监督管理局 FDA 提交事先通知 PN(Prior notice)。第 801(m) 条(Section 801(m))还规定,如果某食品货物在抵达美国目的港(Port of arrival)时,其事先通知不充分(Inadequate)(例如:未提交事先通知、事先通知信息不准确,或未按规定时限提交),则该食品货物依据本法案第 801(m)(1) 条的规定可被拒绝入境,并且不得交付给进口商、所有者或收货人。若某食品货物依据第 801(m)(1) 条的规定被拒绝入境,除非获得美国海关和边境保护局 CBP 同意并在其监管下立即从入境口岸出口,否则该食品必须被扣留在该入境口岸(Port of entry),除非 CBP 或 FDA 另有指示。
Bioterrorism Act 法案第 305 条还在《联邦食品、药品和化妆品法案》中新增了第 415 条(Section 415),要求凡在美国境内或境外从事供人类或动物食用食品的制造、加工、包装或储存活动的设施,均须向 FDA 注册。相关实施法规载于《联邦法规汇编》第 21 编第 1.225 至 1.243 条(21 CFR 1.225 - 1.243)。根据该法案第 801(l) 条,如果进口或拟进口至美国的食品来自尚未根据第 415 条完成注册的美国境外设施,则该食品将被扣留,直至该境外设施完成 FDA 注册。若食品依据第 801(l) 条被扣留,除非获得美国海关和边境保护局 CBP 同意并在其监管下立即从入境口岸出口,否则该食品必须被扣留在该入境口岸(Port of entry),除非 CBP 或 FDA 另有指示。
为执行 Bioterrorism Act 法案的规定,2008 年 11 月 7 日,美国食品药品监督管理局 FDA 在《联邦公报》上发布了一项最终规则(Final rule)(事先通知规则)(Prior Notice rule),修订了《联邦法规汇编》第 21 编第 1 部分第 I 子部分(21 CFR Part 1, Subpart I)中的现有要求,规定必须以电子方式向 FDA 提交进口或拟进口至美国的食品(包括动物食品)的事先通知(Prior notice)(73 FR 66294)。该事先通知规则旨在落实《联邦食品、药品和化妆品法案》第 801(m) 条(Section 801(m) of the Federal Food, Drug, and Cosmetic Act)(21 U.S.C. 381(m))的规定,该条款由 2002 年《公共卫生安全和生物恐怖主义防范与应对法案》(Bioterrorism Act)第 307 条(Section 307 of the Public Health Security and Bioterrorism Preparedness and Response Act of 2002)增订(Public Law 107-188),要求 FDA 对进口食品实施事先通知要求。修订后的法规(Regulations)于 2009 年 5 月 6 日生效。
就事先通知而言,“食品”(Food)的含义以《联邦食品、药品和化妆品法案》第 201(f) 条的规定为准,其定义包括:(1)供人类或其他动物食用的食品或饮料;(2)口香糖;以及(3)作为上述食品组成部分的物品。但该定义不包括食品接触物质(Food contact substances)或农药(Pesticides)。 以下情形不受食品事先通知(Prior Notice)要求的约束:
2,由个人在其私人住所内制作,并由该个人作为私人礼物(即非商业用途)寄送给美国境内其他个人的食品;
3,进口后即出口,且在出口前未离开入境口岸的食品;
4,在进口时依据《联邦肉类检验法案》(Federal Meat Inspection Act)(21 U.S.C. 601 et seq.)受美国农业部 USDA 专属管辖(Exclusive jurisdiction)的肉类食品(Meat food products);
5,在进口时依据《家禽产品检验法案》(Poultry Products Inspection Act)(21 U.S.C. 451 et seq.)受美国农业部 USDA 专属管辖(Exclusive jurisdiction)的家禽产品(Poultry products);
6,在进口时依据《蛋制品检验法案》(Egg Products Inspection Act)(21 U.S.C. 1031 et seq.)受美国农业部 USDA 专属管辖(Exclusive jurisdiction)的蛋制品(Egg products);
7,依据《维也纳外交关系公约》(1961 年)第 27 条第 3 款(Art. 27(3) of The Vienna Convention on Diplomatic Relations)规定,作为外交邮袋内容物运输的食品,即以随身行李或货物形式构成外交邮袋的食品。
2011 年 1 月 4 日签署生效的 FDA《食品安全现代化法案》(FDA Food Safety Modernization Act)旨在通过将联邦监管机构的工作重点从应对污染转向到预防污染来确保美国食品供应的安全。FSMA 第 304 条(Section 304 of FSMA)修订了《联邦食品、药品和化妆品法案》第 801(m) 条(Section 801(m) of the Federal Food, Drug, and Cosmetic Act)(21 U.S.C. 381(m)),要求在向 FDA 提交的进口食品事先通知 PN(Prior notice)中提供额外信息(Additional information)。
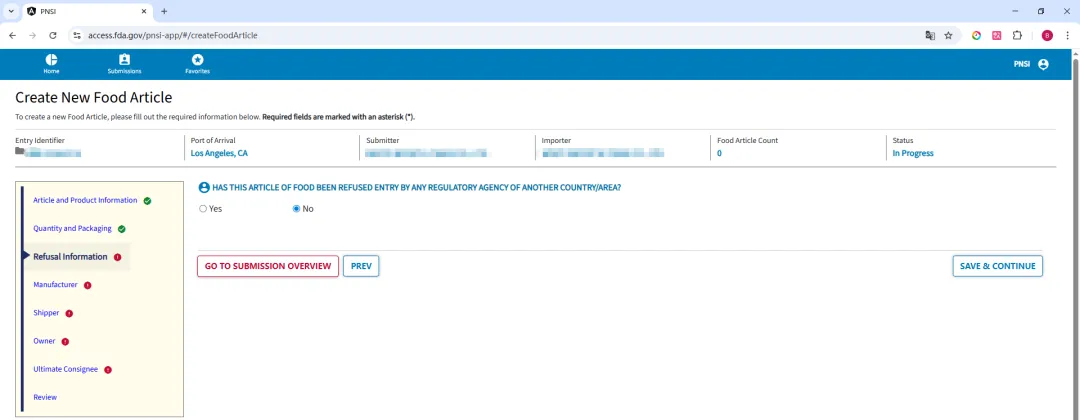
FDA 进口食品事先通知 PN 须报告任何曾拒绝该食品入境的国家/地区的名称
2011 年 5 月 5 日,美国食品药品监督管理局 FDA 根据《食品安全现代化法案》FSMA 第 304 条(Section 304 of the FDA Food Safety Modernization Act)(Public Law 111-353)发布了一项临时最终规则“进口食品事先通知所需信息”(Information Required in Prior Notice of Imported Food)(76 FR 25542)(2011 年 7 月 3 日生效)。该临时最终规则修订了 FDA 关于进口食品事先通知的规定,要求进口食品事先通知中增加一项信息要素,即提交进口食品事先通知(包括动物食品)的人员,须报告任何曾拒绝该食品入境的国家/地区的名称,FDA 称该新增信息要求有助于其在管理进口到美国的食品潜在风险方面做出更明智的决策。
什么是进口食品事先通知 PN
进口至美国的食品(Food)、药品(Drugs)、医疗器械(Devices)和化妆品(Cosmetics)均受《联邦食品、药品和化妆品法案》(Federal Food, Drug, and Cosmetic Act)的管辖。某些食品,例如低酸罐头食品(Low-acid canned foods)、牛奶(Milk)、鸡蛋(Eggs)、果汁(Juices)、海鲜(Seafood)和婴儿配方奶粉(Infant formula),需满足额外的特定产品监管要求(Specific Food Product Requirements),以确保其安全无害且不受污染。
2002 年的 Bioterrorism Act 法案规定了:
I. 对进口或拟进口至美国的食品货物的事先通知(Prior Notice)要求
II. 在美国境内生产、加工、包装或储存供消费食品的食品设施的注册要求
事先通知 PN(Prior Notice)是指在食品(包括动物食品)抵达美国之前,向美国食品药品监督管理局 FDA 提交的通知,表明该食品正在进口或拟进口至美国。进口食品 PN 的目的是为了让 FDA 能够更有效地在美国入境口岸对进口食品进行有针对性的检查(Inspections)或查验(Examinations),并确定是否存在任何可信信息表明该批进口食品对公众健康(Public health)构成威胁或严重风险。
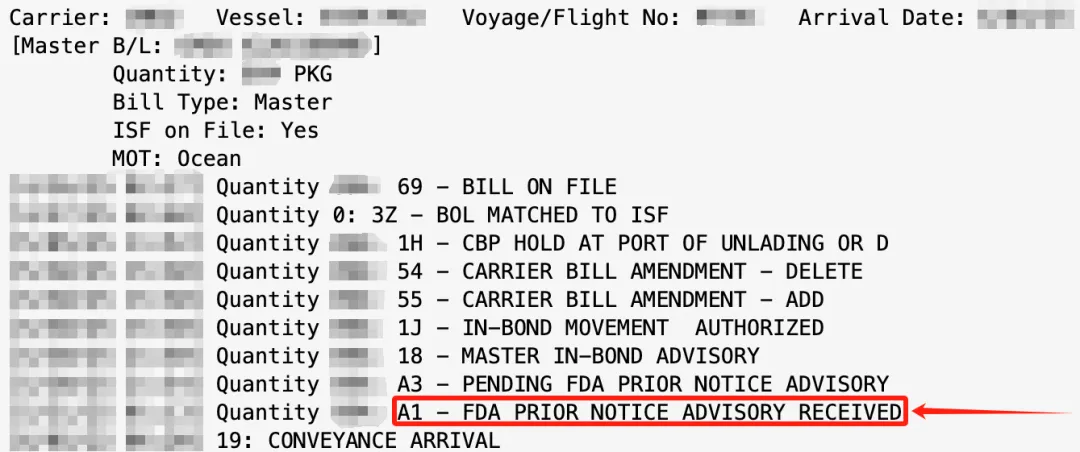
ACE 状态代码 A1:该批货物已向美国食品药品监督管理局 FDA 提交了事先通知 PN
自 2003 年 12 月 12 日起,凡进口至美国的供人类及动物食用的食品,均须向美国食品药品监督管理局 FDA 提交事先通知 PN(Prior Notice),除非该食品属于免于事先通知的豁免范围。
据 FDA 介绍,进口食品货物的事先通知将使 FDA 有时间:
在食品抵达美国之前审查和评估相关信息; 更好地调配资源开展检查(Inspections); 协助拦截受污染产品。
未提交 PN 会使食品进口被拒绝,这可能导致货物(Shipment)被:
在抵达港被扣留(Held at the port of arrival) 转移至安全储存设施,待符合 PN 要求后处理(Moved to secured storage pending compliance with PN requirements) 出口(Exported),或 销毁(Destroyed)
如何提交进口食品事先通知 PN
所有进口或拟进口至美国的供人类和动物食用的食品均须提交事先通知 PN(Prior Notice)(21 CFR, Part 1, Subpart I)。
PN 提交需要提供以下信息:
(a)发货信息(报关信息)(Shipment Information (Entry Information))
提交人(Submitter):正式提交货物信息的个人或实体。 进口商(Importer):进口货物的个人或组织名称。 承运人(Carrier):负责运输货物的公司或个人的名称。 计划发货信息(Planned Shipment Information):有关拟发货的详细信息,包括始发地、目的地、提单、航空运单或跟踪号(如适用)以及任何其他相关的物流信息。
(b)商品信息(Article Information)
产品(Product):所运输食品的描述 数量和包装(Quantity & Packaging):运输的产品数量及其包装方式 相关设施(Related Facilities):关于该产品制造商、托运人、所有者和最终收货人的信息,包括名称、地址和联系方式。
进口食品事先通知(Prior Notice of Imported Food)PN 须通过以下两种方式之一提交:
(1)CBP 的 ABI/ACE 系统:美国海关和边境保护局 CBP(前身为美国海关总署)(U.S. Customs Service)已对其自动化商业环境(Automated Commercial Environment)(ABI/ACE)系统中的自动化报关行接口 ABI(Automated Broker Interface)进行了修改,使申报人可以通过 CBP 与 FDA 之间既有的系统接口,将事先通知 PN 提交至 FDA。
(2)FDA 的 PNSI 系统:事先通知系统接口 PNSI(Prior Notice System Interface)系统适用于无法(例如在 ACE/OASIS 系统接口不可用时)或选择不通过 CBP 提交事先通知的相关方。
PNSI 可通过 FDA 行业系统 FIS(FDA Industry Systems)访问:https://www.access.fda.gov/,
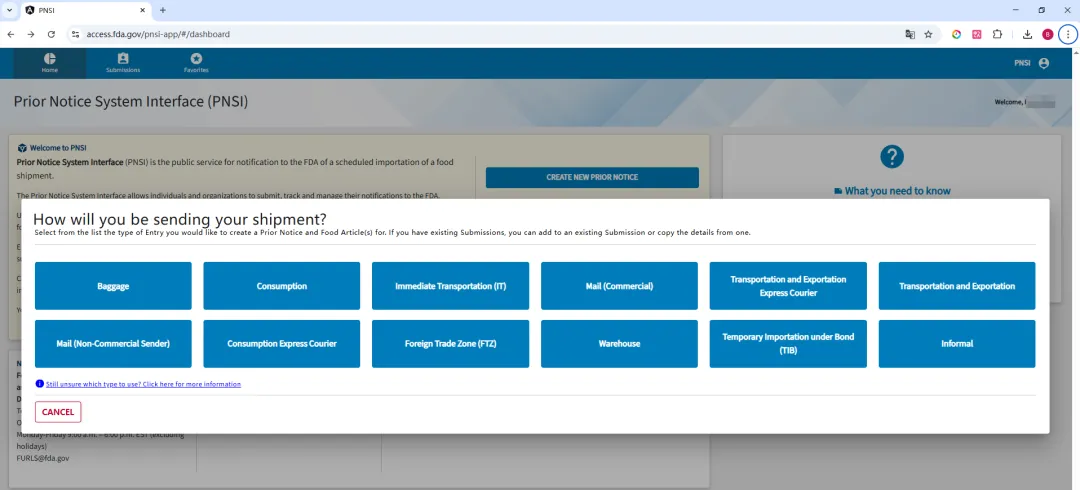
登录后,选择需要提交 PN 的货物报关类型,
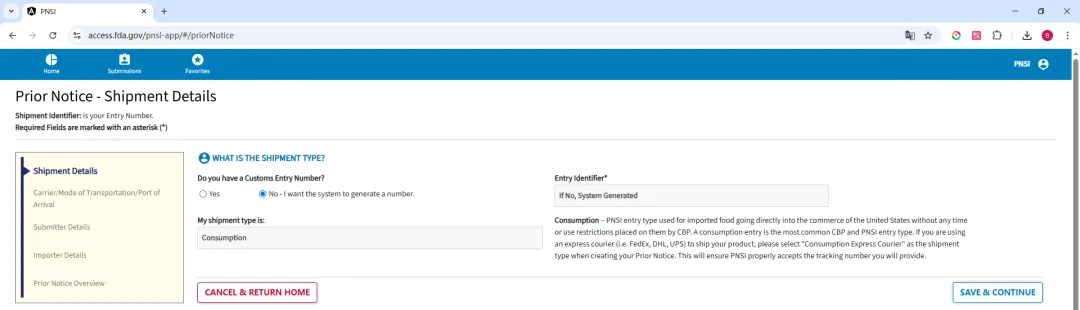
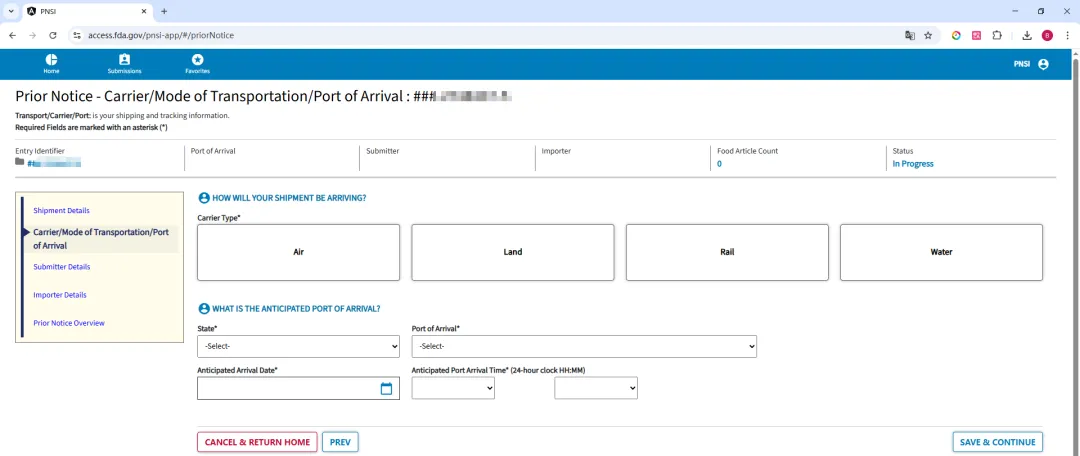
然后按页面提示填写 PN 信息,
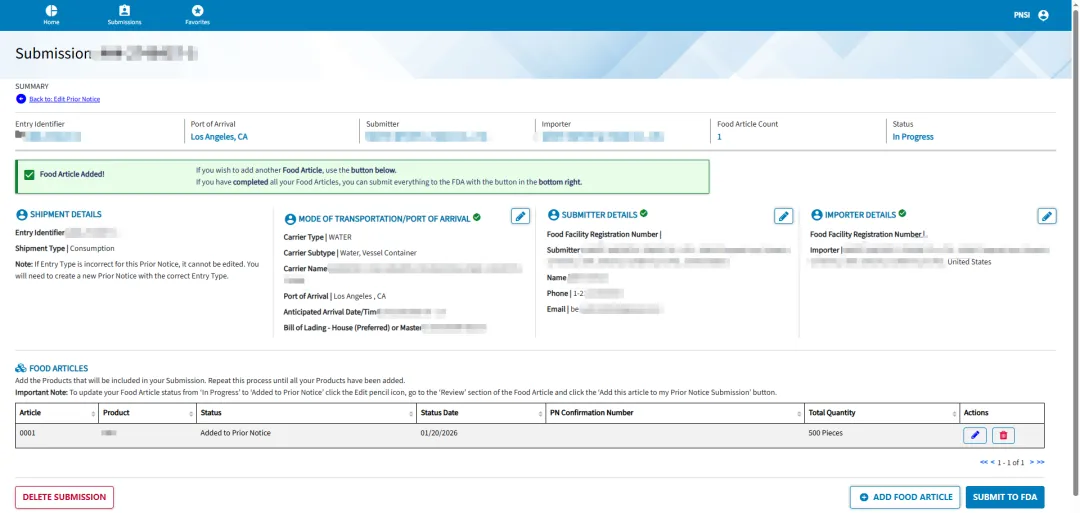
全部填写完毕,最后确认无误,点击 SUBMIT TO FDA 提交至 FDA,
无论采用何种传输方式向 FDA 提交,事先通知信息均需在 FDA 的进口支持运营与管理系统 OASIS(Operational and Administrative System for Import Support)中接受验证流程及筛查,以确保符合食品安全与保障标准。若 FDA 系统判定无需对该事先通知或食品进行进一步评估或采取行动,系统将通过 OASIS 向美国海关 CBP 的 ABI/ACE 电子申报接口发送通知,表明该食品可有条件放行(Conditionally released)。但是,如果需要对事先通知信息进行额外评估(Additional evaluation),FDA 的 PNC 工作人员将查阅所提供的信息,判断其是否存在对公共健康构成重大风险的潜在可能。
美国食品药品监督管理局 FDA 设立了目标锁定与分析处 DTA(Division of Targeting and Analysis),以执行 2002 年《公共卫生安全和生物恐怖主义防范与应对法案》BTA(Public Health Security and Bioterrorism Preparedness and Response Act of 2002)赋予的权力。DTA 负责分析食品进口事先通知信息,以评估进口供人类或动物食用食品在运输或进口过程中遭受人为恶意污染的风险;并与相关执法机构(如 CBP)保持联络,获取并应对有关拟进口至美国的潜在危险人类或动物食品产品的执法情报;同时,确保《联邦法规汇编》第 21 编中 I 分章(Title 21 Code of Federal Regulations, Subpart I)(进口食品的事先通知)(Prior Notice of Imported Foods)及 H 分章(Title 21 Code of Federal Regulations, Subpart H)(食品设施注册)(Registration of Food Facilities)的监管要求得到遵守。
进口食品事先通知 PN 常见问题解答
什么是进口食品事先通知 PN(Prior notice)?
事先通知 PN(Prior Notice)是指在食品(包括动物食品)抵达美国之前,向美国食品药品监督管理局 FDA 提交的通知,表明该食品正在进口或拟进口至美国。
所有进口到美国的食品的制造商或加工商都必须在 FDA 进行有效的食品设施注册备案。注册信息是 FDA 事先通知中必需的数据(Required data)。
需要提交事先通知 PN 的进口食品包括:
所有进口或提供进口到美国的食品 在美国储存或分销的进口食品 用作礼品、贸易物品和质量保证/控制样品的进口食品 经美国转运至其他国家的进口食品 为将来出口而进口到美国的食品 准许进入美国对外贸易区 FTZ(U.S. Foreign Trade Zone)的进口食品
为什么需要向 FDA 提交事先通知 PN?
根据《联邦食品、药品和化妆品法案》第 801(m) 条(Section 801(m) of the FD&C Act)(21 U.S.C. 381(m))及其在《联邦法规汇编》第 21 编第 1 部分第 I 子部分(21 CFR part 1, subpart I)中的实施条例(Implementing regulation)规定,必须提交事先通知 PN(Prior notice)。
《联邦食品、药品和化妆品法案》第 801(m) 条(Section 801(m) of the FD&C Act)规定,进口或拟进口至美国的食品在抵达美国前必须向美国食品药品监督管理局 FDA 进行预先通知(Aadvance notification)。
事先通知 PN 要求何时生效?
进口食品事先通知要求随着 FDA“事先通知临时最终规则”(68 FR 58974,2003 年 10 月 10 日)的发布而于 2003 年 12 月 12 日正式生效。
就事先通知 PN 规则而言,何为“食品”(Food)?
《联邦法规汇编》第 21 编第 1.276 条(21 CFR 1.276)援引《联邦食品、药品和化妆品法案》第 201(f) 条(Section 201(f) of the FD&C Act)对“食品”(Food)进行了定义,该条将“食品”定义为供人类或其他动物食用或饮用的物品、口香糖以及作为上述物品组成部分的物品(21 U.S.C. 321(f))。然而,就事先通知而言,“食品”的定义不包括食品接触物质或农药(21 CFR 1.276(b)(5)(i))。须提交事先通知的“食品”示例包括但不限于:鱼类及海产品(Fish and seafood)、活体食用动物(Live food animals)、乳制品(Dairy products)、带壳鸡蛋(Shell eggs)、水果(Fruits)、蔬菜(Vegetables)、用作食品或作为人类和动物食品(包括宠物食品)组成部分使用的初级农产品(Raw agricultural commodities)、食品配料(Food ingredients)、食品添加剂(Food additives)、婴儿配方食品(Infant formula)、饮料(包括酒精饮料和瓶装水)、烘焙食品(Bakery goods)、零食(Snack foods)、糖果(Candy)、罐头食品(Canned foods)、膳食补充剂及膳食成分(Dietary supplements and dietary ingredients)。
事先通知 PN 规则的适用范围是什么?哪些进口或拟进口至美国的食品需要提交事先通知?
如果运往美国的货物属于《美国联邦法规汇编》第 21 编第 1.276(b)(5) 条(21 CFR 1.276(b)(5))所定义的食品范畴,则通常需要提交事先通知,即使该物品拟用于进一步加工、并非拟在美国消费或并非拟用于商业分销。因此,除非明确适用法规规定的豁免情形,否则凡供人类或其他动物食用的食品,只要进口或拟进口至美国,用于在美国境内使用、储存或分销,均须提交事先通知 PN,包括作为礼品的食品、贸易样品和质量保证/质量控制样品、经美国转运至其他国家的食品、为未来出口而进口至美国的食品,以及获准进入美国保税区 FTZ(Foreign Trade Zone)的进口食品。
是否存在免于提交事先通知 PN 的情形?
是。根据《联邦法规汇编》第 21 编第 1.277(b) 条(21 CFR 1.277(b))的规定,下列情形无需提交事先通知:
(a)个人自用食品,即供本人、家庭成员或朋友食用且不用于销售或其他分销的食品,在个人入境美国时由本人随身携带或伴随入境;
(b)由个人在其私人住所中制作,并由该个人以个人礼品(即非商业用途)形式寄送给美国境内其他个人的食品;
(c)进口后在未离开到达港口(Port of arrival)的情况下即予以出口(Immediately exported)的食品(即保税报关类型 63)(IE, in-bond type 63);
(d)在进口时属于美国农业部 USDA 专属管辖范围(Exclusive jurisdiction)的肉类食品、禽类产品及蛋制品;以及
(e)适用 1961 年《维也纳外交关系公约》第 27 条第 3 款(Article 27(3) of the Vienna Convention on Diplomatic Relations)规定的食品,即作为外交邮袋行李或货物运输的食品。
如果食品不供在美国境内消费,是否需要提交事先通知 PN?
是。即使食品不供在美国境内消费,也需要提交事先通知。对于用于转运、进一步加工和出口或储存和出口的食品,都必须提交事先通知(参见 21 CFR 1.277(a))。
通过国际邮件(International mail)进口至美国的食品是否可免于提交事先通知 PN?
否。除非适用《联邦法规汇编》第 21 编第 1.277(b) 条(21 CFR 1.277(b))规定的豁免情形,否则通过国际邮件进口的食品须提交事先通知,该通知必须在食品寄往美国之前提交(21 CFR 1.279(c))。
如果由个人在其私人住所制作的食品,或者个人从商家/供应商(Vendor)购买后,由该个人以“私人礼品(非商业用途目的)”(Personal gift)形式寄送给美国境内个人的食品,则不受 BTA 法案要求的约束。
但是,如果食品是由商家(Business)直接寄送给美国境内个人的,则须遵守 FDA 的特别规定(Special requirements)。例如:
如果你在英国一家食品店购买礼品篮,然后你自己带去邮局或快递公司寄给朋友 —— 不受 BTA 法案要求的约束; 但如果你在同一家店要求商家代为寄送礼品篮 —— 则该货物(Shipment)适用 BTA 要求,商家必须提交事先通知 PN(Prior Notice)。
食品经美国转运出口至其他国家时,是否需要提交事先通知 PN?例如,通过 T&E 报关入境(Transportation and Exportation entry)?
是。食品经美国转运出口至其他国家以及食品用于未来出口均需提交事先通知(21 CFR 1.277(a))。
对于受美国农业部管辖的肉类、家禽或蛋制品,是否需要提交事先通知 PN?
如果进口或拟进口至美国的食品受美国农业部 USDA《联邦肉类检验法案》(Federal Meat Inspection Act)(21 U.S.C. 601 et seq.)、《家禽产品检验法案》(Poultry Products Inspection Act)(21 U.S.C. 451 et seq.)或《蛋制品检验法案》(Egg Products Inspection Act)(21 U.S.C. 1031 et seq.)的专属管辖(Exclusive jurisdiction),则该食品不受事先通知要求的约束(21 CFR 1.277(b)(4)-(b)(6))。
如何向 FDA 提交事先通知 PN?
必须通过美国海关和边境保护局 CBP 的 ABI/ACE/ITDS 系统或美国食品药品监督管理局 FDA 的 PNSI 系统,以电子方式向 FDA 提交事先通知。
CBP 的自动化报关行接口/自动化商业环境/国际贸易数据系统 ABI/ACE/ITDS(Automated Broker Interface/Automated Commercial Environment/International Trade Data System)允许通过现有的 ABI/ACE/ITDS 电子申报接口(Interface)向 FDA 提交事先通知(21 CFR 1.280(a)(1)) FDA 的事先通知系统接口 PNSI(Prior Notice System Interface)可通过:https://www.access.fda.gov/ 访问(21 CFR 1.280(a)(2))。对于通过国际邮件(International mail)进口或拟进口的食品,以及无法通过 ABI/ACE/ITDS 系统进行的其他申报事务类型(Transaction types),必须通过 FDA PNSI 提交进口食品事先通知。
你必须获得授权才能使用 CBP 的 ABI/ACE/ITDS 接口(19 CFR 143.1),进口商可以委托报关行代为发送,但任何人都可使用 FDA 的 PNSI 系统。若你是 ABI/ACE/ITDS 的授权用户,可在向CBP 提交入境申报(Entry)时一并提供事先通知。
我是否需要同时向 FDA 和 CBP 提交事先通知 PN?
否。必须向 FDA 提交事先通知。如果你是美国海关和边境保护局 CBP 的 ABI/ACE/ITDS 系统的授权用户,可以通过 ABI/ACE/ITDS 电子申报接口向FDA提交事先通知。如果你不是美国海关 ABI/ACE/ITDS 系统的授权用户,可以安排授权用户提交事先通知,或者你也可以通过 FDA PNSI 系统提交。
我是 CBP 系统 ABI/ACE/ITDS 的授权用户。我可以使用 FDA PNSI 提交事先通知 PN 吗?
是。你可以通过任一系统提交事先通知。
在未提交事先通知 PN 的情况下,是否可以为食品向美国海关和边境保护局 CBP 提交进口报关(Entry)或入境申请(Admission)?
否。如果报关或入境申请中包含受事先通知要求约束的食品,则在未向 FDA 提交该食品的事先通知之前,不得向 CBP 提交进口报关或入境申请。这是因为协调关税表 HTS 编码已被系统标记,用以识别需要或可能需要提交事先通知的食品。
事先通知 PN(Prior notice)必须通过以下两种方式之一提交:一是通过 CBP 的 ABI/ACE/ITDS 系统,与 CBP 报关信息(Entry information)一并提交;二是通过 FDA 的 PNSI 系统(21 CFR 1.280(a))。
若通过 FDA 的 PNSI 系统提交事先通知,提交成功后将收到一个事先通知确认号(PN Confirmation Number)(21 CFR 1.279(d))。如随后通过 CBP 的 ABI/ACE/ITDS 系统提交进口报关或入境申请,则必须在报关时以合规性声明(Affirmation of Compliance)的形式填报该 PN 确认号。该 PN 确认号使 CBP 能够确认相关食品已依法向 FDA 提交了事先通知。
对于属于即时运输 IT(Immediate Transportation)或运输和出口 T&E(Transportation and Exportation)报关类型的食品,我该如何提交事先通知 PN?
美国海关和边境保护局 CBP 已对 ABI/ACE/ITDS 电子申报接口进行了修改,允许 IT 和 T&E 报关的食品货物向 FDA 提交事先通知。此类报关的食品货物的事先通知也可通过 FDA PNSI 系统提交。
事先通知 PN 必须在何时提交?
提交事先通知 PN 的时间要求取决于运输方式和目的港(Port of arrival),即食品首次抵达美国的口岸(此口岸可能与向美国海关 CBP 提交报关的口岸不同),具体而言,除通过国际邮件寄送的食品外,事先通知必须在以下最短时间之前提交,并且提交后须已获得 FDA 的确认:
若食品通过公路方式入境,须在到达目的港(Port of arrival)前不少于 2 小时; 若食品通过铁路方式入境,须在到达目的港(Port of arrival)前不少于 4 小时; 若食品通过空运方式入境,须在到达目的港(Port of arrival)前不少于 4 小时; 若食品通过海运方式入境,须在到达目的港(Port of arrival)前不少于 8 小时(21 CFR 1.279(a))。
如通过 CBP 的 ABI/ACE/ITDS 系统提交事先通知,不得早于预计到达日期前 30 个日历日提交(21 CFR 1.279(b)(1));如通过 FDA 的 PNSI 系统提交,则不得早于预计到达日期前 15 个日历日提交(21 CFR 1.279(b)(2))。
对于通过国际邮件寄送的食品,事先通知必须在食品寄出之前提交并获得 FDA 确认(21 CFR 1.279(c)),且事先通知确认号必须填写在随包裹附带的海关申报单上(Customs Declaration)(21 CFR 1.279(e))。
如个人随身携带食品或食品伴随个人入境(例如放在托运行李或车辆后备箱中),且该食品并非供个人使用,则必须按照所使用的运输方式,在相应的时间框架(Timeframe)内提交事先通知,并在入境时获得 FDA 的确认,并向 CBP 或 FDA 提供包括预先通知确认号在内的确认文件(21 CFR 1.279(f))。












































